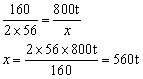| 金属资源的利用和保护(1) |
主讲: 化学高级教师 舒宝生
引入:地球上的金属资源是有限的,故我们需要对其进行合理的利用和有效的保护。
一、常见的矿石
工业上把能用来提炼金属的矿物叫做矿石。
展示:
思考:
1、你能说出几种常见矿石的主要成分吗?
矿石
赤铁矿
磁铁矿
黄铁矿
铝土矿
主要成分
2、Fe2O3、Fe3O4、FeS2、FeO炼铁,哪一种矿石较好?
(1)FeS2炼铁过程中会产生SO2,污染空气;
(2)Fe2O3、Fe3O4、FeO中含铁元素的质量分数由大到小的关系为:FeO>Fe3O4>Fe2O3。
二、铁的冶炼
说明:炼铁的原理是利用一氧化碳把铁从铁矿石里还原出来。
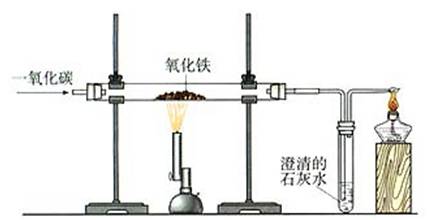
展示:一氧化碳还原氧化铁的装置图:
现象:红色粉末逐渐变为黑色粉末,澄清的石灰水变浑浊,尾气燃烧产生蓝色火焰。
方程式:Fe2O3+3CO
2Fe+3CO2
实验注意事项:(1)用酒精喷灯加热;(2)尾气处理。
思考:若将氧化铁换成四氧化铁,主要化学方程式怎样?
Fe3O4+4CO
3Fe+4CO2
展示:
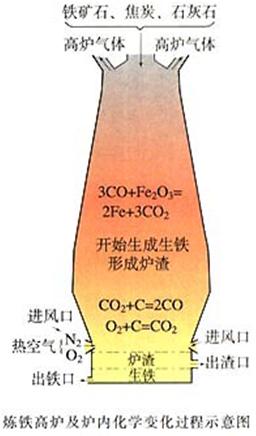
总结:工业炼铁
1、原料:铁矿石、焦炭、 石灰石、空气
2、主要反应:
Fe2O3+3CO
2Fe+3CO2
Fe3O4+4CO
3Fe+4CO2
过渡:工业炼铁是利用焦炭与氧气反应生成的CO把铁从铁矿石里还原出来。
3、其它反应
C+O2
CO2; CO2+C
2CO
石灰石:将矿石中的SiO2转变为炉渣。
焦炭:①产生热量;②产生一氧化碳。
4、设备:高炉
5、产品:生铁
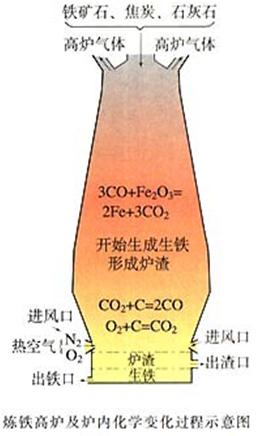
展示:
思考:为什么高炉的出渣口比出铁口高?
炉渣的密度比生铁的密度小。
三、含杂质物质的化学方程式的计算
注意问题:
1、化学方程式能表达的都是纯净物之间的质量关系。
2、当化学反应中的物质含有杂质时,先把含杂质的物质的质量换算成纯物质的质量,再进行计算。
例1、用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁多少吨?
解:
1000t赤铁矿石中含氧化铁的质量为
1000t×80%=800t
设:800t氧化铁理论上可以炼出铁的质量为x。
Fe2O3+3CO
2Fe+3CO2
160 2×56
800t x
折合为含铁96%的生铁的质量为560t÷96%=583t
答:1000t含氧化铁80%的赤铁矿石,理论上可炼出含铁96%的生铁583t。
例2、冶炼2000t含杂质3%的生铁,需要含Fe3O490%的磁铁矿石多少吨?
解:
2000t含杂质3%的生铁中铁的质量为:
2000t×(1-3%)=1940t
设:需要磁铁矿石的质量为x
Fe3O4+4CO
3Fe+4CO2
232 168
x×90% 1940t
x=2976.7t
答:需要磁铁矿石的质量为2976.7t。
例3、含杂质25%的大理石20g与足量的盐酸反应,(杂质与盐酸不反应)可生成二氧化碳多少克?
解:
20g大理石中含CaCO3的质量为:20g×(1-25%)=15g
设可生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
15g x
x=6.6g
答:可生成二氧化碳6.6g。
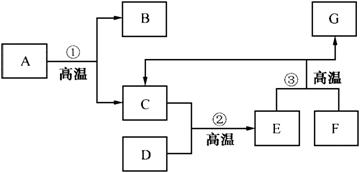
例4、工业上以大理石和赤铁矿为主要原料可以制取B和G,其转化关系如下图所示,已知D、G的主要成分为单质。试回答下列问题:
(1)写出工业制取的两种物质的化学式:
B__________、G__________。
(2)写出下列反应的化学方程式:
反应②:__________;
反应③:__________;
检验气体C:__________。
答案:
(1)CaO; Fe
(2)CO2+C
2CO
Fe2O3+3CO
2Fe+3CO2
CO2+Ca(OH)2=CaCO3↓+H2O
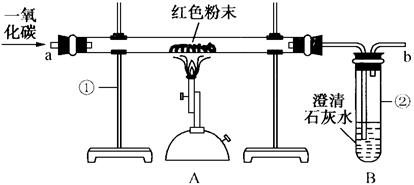
例5、如下图是课堂中模拟炼铁的实验装置。
(1)写出图中标有序号的仪器名称:
①__________;②__________。
(2)实验过程中,先要进行的是__________。(填Ⅰ或Ⅱ)
Ⅰ.加热 Ⅱ.通一氧化碳
(3)A、B中反应的化学方程式分别是____________________。B中观察到的现象是____________________。
(4)该装置的不足之处是__________。
解析:
掌握炼铁的实验原理。
答案:
(1)铁架台;试管
(2)Ⅱ
(3)3CO+Fe2O3
2Fe+3CO2;
CO2+Ca(OH)2=CaCO3↓+H2O;澄清石灰水变浑浊
(4)没有尾气处理装置
总结:
一、常见的矿石
二、铁的冶炼
1、原料:铁矿石、焦炭、石灰石、空气
2、主要反应
Fe2O3+3CO
2Fe+3CO2
Fe3O4+4CO
3Fe+4CO2
三、含杂质物质的化学方程式的计算
- 返回 -