| 金属资源的利用和保护(2) |
主讲: 化学高级教师 舒宝生
创设情景:
资料一:一方面,我们每年要向自然界索取大量的金属矿物资源,用来冶炼金属;另一方面,据有关资料报道,现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。
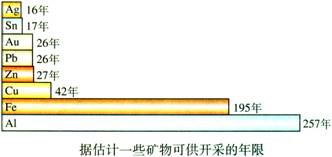
矿物的储量有限,而且不能再生,根据已探明的一些矿物的储藏量,并根据目前这些金属的消耗速度,有人估计一些矿物可供开采的年限如图所示:
引入:金属资源短缺和金属腐蚀对人类是一种挑战,因此,保护金属资源很重要。
一、金属的腐蚀和防护
过渡:金属腐蚀是需要条件的;首先我们一起探究铁制品锈蚀的条件及防锈措施。
1、铁制品的锈蚀条件
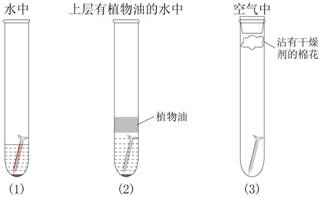
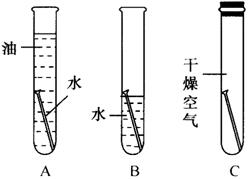
展示:
现象:
(1)中,铁钉生锈,且铁在空气、水的界面处生锈严重;
(2)中,铁钉(基本上)不生锈;
(3)中,铁钉(基本上)不生锈。
结论:铁与水和氧气同时接触,铁才会生锈。
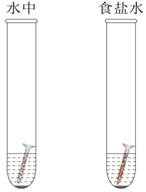
展示:
现象:浸没在食盐水中的铁钉比浸没在水中的铁钉锈蚀更严重。
铁生锈的条件:铁与氧气(或空气)和水同时接触。
NaCl和酸能加速铁的锈蚀。
注意:(1)铁锈的主要成分是Fe2O3·x H2O,铁锈疏松多孔,铁制品可以全部锈蚀。
(2)钢铁在空气中锈蚀,是铁与空气中的氧气和水共同作用。
思考:(1)铁锈的颜色怎样?它是纯净物吗?氧化铁能像铝表面的氧化铝薄膜一样阻止铁的锈蚀吗?
铁锈是红色的,属于混合物,主要成分是Fe2O3·x H2O;铁锈是疏松多孔的,铁制品可以全部锈蚀,而氧化铝薄膜是致密的,能保护里层的铝。
(2)探究铁生锈的条件中为何要用煮沸后冷却的蒸馏水?
过渡:如何防止铁制品生锈呢?
2、铁制品的防锈措施
(1)保持铁制品表面清洁、干燥。
(2)在铁制品表面覆盖保护膜,如涂油、刷漆、电镀、烤蓝等。
(3)改变金属的内部结构,如制成不锈钢。
说明:破坏铁制品锈蚀的条件,使铁制品隔绝空气和水,就能防止铁制品生锈。
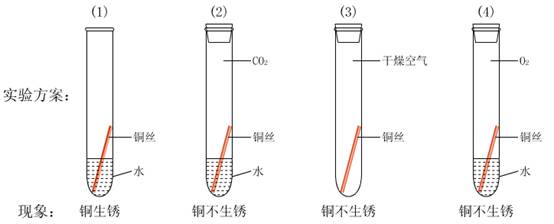
3、铜生锈条件的探究(控制变量对比的方法)
铜生锈的条件:铜与氧气、水、二氧化碳共同接触。
2Cu+O2+H2O+CO2=Cu2(OH)2CO3
设计的实验:
实验方案:
过渡:对于金属资源,除了采取措施防止金属的腐蚀,还有什么途径可以保护金属资源?
二、金属资源的保护
1、防止金属的腐蚀;
2、回收和利用废旧金属:
①经济,可降低生产成本;
②节省金属资源和能源;
③减少污染(如:重金属)
3、有计划、合理地开采矿物;
4、寻找金属的代用品。
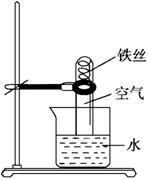
例1、如图所示实验,装置中出现的现象是( )
A.铁丝不变化
B.铁丝逐渐消失
C.试管中的液面不变化
D.试管中的液面上升
解析:
铁生锈的条件是:铁与O2、水接触,试管中氧气消耗,试管中的液面上升。
答案:D
例2、钢铁是人类生活和生产中非常重要的材料,但全世界每年都有约相当于年产量四分之一的钢铁因生锈损失。某化学课外活动小组,对钢铁制品锈蚀的条件进行如下探究,设计了如图所示的实验,据此回答下列有关问题:
(1)一周后,观察到编号为__________的试管中的铁钉锈蚀严重。
(2)常温下,铁生锈的条件是铁跟__________和__________等物质相互作用的结果,铁锈的主要成分是__________(用化学式表示)。
(3)欲除去铁锈,同学们提出了三种不同的实验方法:①用砂布擦;②用稀盐酸洗;③用稀碱液泡。你认为最有效的方法是__________(填序号)。
(4)如何防止家庭中常用的铁制品生锈,简单易行的方法有(列举一种方法):__________。
解析:
解题的关键是能依据实验目的,用比较的方法和用控制变量的思维方法得出钢铁生锈的条件:同时有水和空气。由此出发,联系所学的基础知识即可解答本题。
答案:(1)B
(2)水(或H2O) 氧气(或O2) Fe2O3
(3)②
(4)保持铁制品的洁净和干燥;擦干后涂油等(其他合理的方法均可)
例3、人类生活离不开金属。
(1)铁是生活中常用的金属。如图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热。
①发热剂需接触到空气才会发热,原因是铁要与__________、__________等物质共同作用才会生锈。
②推测发热剂成分中氯化钠的作用是____________________。
(2)应用金属活动性顺序能帮助我们进一步学习金属性质。已知下列各组物质间均能发生置换反应。
A.Fe和CuSO4溶液
B.Mg和MnSO4溶液
C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式____________________。
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序____________________。
答案:
(1)①水、氧气
②加速铁粉生锈,更快的放出热量
(2)①Fe+CuSO4=FeSO4+Cu
②Mg>Mn>Fe>Cu
总结:
1、铁制品生锈的条件
2、铁制品的防锈措施
3、铜生锈的条件
4、保护金属资源的措施
- 返回 -