1、把10g氯化钠放入40g水中,完全溶解后,溶液中氯化钠的质量分数为( )
A.10% B.20%
C.25% D.33.3%
2、将100 g10%的某固体物质M的溶液,分别进行下述操作,所得溶液中溶质的质量分数最小的是( )
A.蒸发掉10 g水,无晶体析出 B.加入10 g10%的M的溶液
C.加入10 g固体M,并使之完全溶解 D.加入10 g水
3、20℃时,向一杯不饱和的KNO3溶液中逐步加入KNO3晶体(温度保持不变,水分蒸发不计)。下列图象能表示这一过程中,溶液溶质质量分数随加入的KNO3晶体质量而变化的是( )
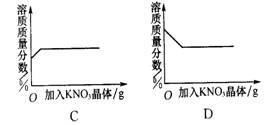
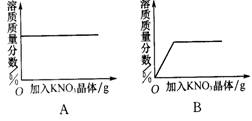
4、现有40 g溶质质量分数为5%的硝酸钾溶液,若将其溶质质量分数增加到10%,应采用的方法是( )
A.蒸发掉19 g溶剂 B.加入2 g硝酸钾
C.加入40 g15%的硝酸钾溶液 D.加入40 g5%的硝酸钾溶液
5、有100 g 5%的氯化钠溶液,若将其溶质的质量分数增大一倍,可采用的方法是( )
A.把溶剂蒸发掉一半 B.加入5 g氯化钠固体
C.把溶剂蒸发掉50 g D.加入100g 5%氯化钠溶液
6、下列做法能改变溶液中溶质质量分数的是( )
A.将氯化铵的饱和溶液降温
B.将硝酸钾的饱和溶液升温
C.把氯化钠的饱和溶液恒温蒸发
D.在蔗糖的饱和溶液中再加少量蔗糖
7、下列关于溶液的说法错误的是( )
A.饱和溶液析出晶体后,其溶质的质量分数可能不变
B.在溶液里进行的化学反应,通常比较快
C.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
D.不饱和溶液转化为饱和溶液,溶质质量分数可能不变
8、20℃时,NaCl溶解于水的实验数据如下表。则下列叙述正确的是( )
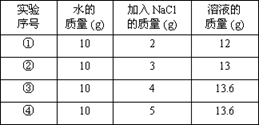
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
9、现有60℃的饱和NaCl溶液,与该溶液有关的量有:①水的质量;②溶液中溶质NaCl的质量;③NaCl的质量分数;④60℃时NaCl的溶解度:⑤溶液的质量。用序号填空:
(1)将该饱和溶液稀释,不变的量有:______________;
(2)将该饱和溶液降温至20℃,一定变化的量有______________。
10、下面的表格中列出了NH4Cl在不同温度下的溶解度:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
溶解度/g |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
(1)由上表可推出溶解度曲线的变化规律是______________;
(2)在20℃时,向100 g水中加入50 gNH4Cl,形成的______________(填“饱和”或“不饱和”)溶液,将其温度升高到60℃时,该溶液中溶质与溶剂的质量比为______________。