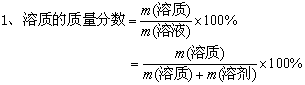| 溶质的质量分数(3) |
主讲: 化学高级教师 舒宝生
复习:
2、溶解度
(1)定义:
(2)饱和溶液中,溶质、溶剂与溶解度的关系
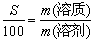
3、有关溶质的质量分数的计算
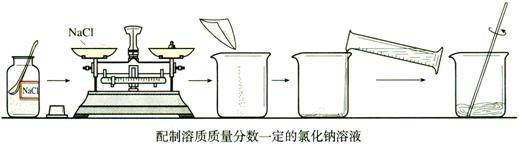
一、配制溶质的质量分数一定的溶液
例:1、计算配制50g质量分数为6%的氯化钠溶液所需氯化钠和水的质量:氯化钠__________g,水__________g。
2、用托盘天平称量所需的氯化钠,倒入烧杯中。
3、把水的密度近似看做1g/cm3。用量筒量取所需的水,倒入盛有氯化钠的烧杯里,用玻璃棒搅拌,使氯化钠溶解。
4、把配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(标签中应包括药品名称和溶液中溶质的质量分数),放到试剂柜中。
总结:配制溶质的质量分数一定的溶液的步骤和主要仪器
步骤 主要仪器
1、计算
2、称量 托盘天平、药匙、量筒、胶头滴管
3、溶解 玻璃棒、烧杯
4、装瓶贴签
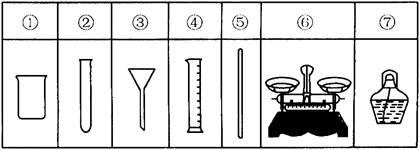
例1、用氯化钠固体配制50g质量分数5%的氯化钠溶液,下列仪器中需要用到的是( )
A.②④⑥⑦ B.①④⑤⑥
C.①③⑤⑦ D.①③④⑥
答案:B
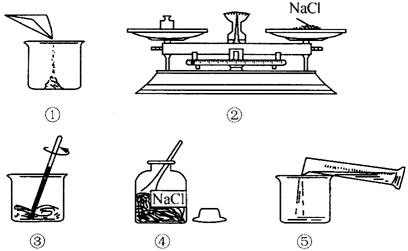
例2、下图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图。
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、__________、__________、量筒。
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果________________。
(3)图②、图③表示的操作步骤分别是____________________。
(4)配制时需称量氯化钠__________g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数__________(填“偏大”或“偏小”);量取水最好选择__________的量筒(填序号①10mL ②50mL ③100mL)(水的密度为1g/cm3)。
(5)下列错误操作可能导致溶液溶质质量分数小于12%的是__________(填序号)。
①B操作时食盐和砝码位置颠倒了
②A操作中有固体洒落
③用量筒量取蒸馏水时,仰视凹液面最低处读数
④E操作中有少量水洒出
⑤C操作中有溶液洒出
答案:
(1)烧杯;玻璃棒
(2)氯化钠和砝码位置放反,造成称量不准(或量筒中的水没有沿烧杯内壁倒入,造成液滴飞溅)
(3)称量和溶解
(4)12.0;偏小;③
(5)①②③
二、溶液的浓、稀与饱和、不饱和的关系
溶液的浓或稀可用溶质的质量分数表示,溶质的质量分数越大,溶液越浓;溶质的质量分数越小,溶液越稀。
饱和与不饱和是指能否继续溶解溶质,与溶解度有关。
1、浓溶液不一定是饱和溶液,饱和溶液也不一定是浓溶液。
稀溶液不一定是不饱和溶液,不饱和溶液也不一定是稀溶液。
2、同种溶质的饱和溶液一定比它的不饱和溶液的浓度大。
三、溶质的质量分数与溶解度的比较
|
溶解度 |
溶质的质量分数 |
意义 |
一定温度时,100g溶剂中最多能溶解溶质的质量。 单位:g |
溶质的质量与溶液的质量之比 |
作用 |
表示某物质溶解能力的大小 |
表示溶液的组成(即浓度的大小) |
条件 |
一定温度[一定压强(气体)] |
一般与温度无关 |
状态 |
饱和状态 |
不一定饱和 |
计算式 |
|
|
相互联系:
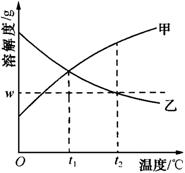
例3、如图是甲、乙两种物质的溶解度曲线。在t2℃时往盛有100g水的烧杯中先后加入wg甲和wg乙(两种物质溶解时互不影响,且溶质仍是甲、乙),充分搅拌。将混合物的温度降低到t1℃。下列说法正确的是( )
A.甲物质的溶解度随温度升高而减小
B.乙物质的溶解度随温度升高而增大
C.温度降低到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的不饱和溶液
D.t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液
解析:
t1℃时,甲、乙的溶解度都大于w g,说明此时溶质的质量分数都为
×100%。
答案:C
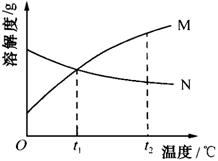
例4、下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是( )
A.t1℃时,M、N两物质溶液溶质质量分数相等
B.由t1℃升温到t2℃时,N物质溶液溶质质量分数不变
C.M物质的溶解度大于N物质的溶解度
D.N物质的溶解度随温度的升高而降低
解析:
A中,t1℃时,M、N两物质饱和溶液溶质质量分数相等;B中,由t1℃升温到t2℃时,N物质若析出,溶液溶质质量分数会减小;C中,温度大于t1℃时,M物质的溶解度大于N物质的溶解度。
答案:D
总结:
一、配制溶质的质量分数一定的溶液的方法
二、溶液的浓、稀与饱和、不饱和的关系
三、溶质的质量分数与溶解度的关系

- 返回 -