1、用氯化钠配制100 g溶质质量分数为20%的氯化钠溶液,现有下列操作:①溶解;②称取氯化钠;③过滤;④量取水;⑤计算;⑥蒸发结晶。正确的操作顺序是( )
A.①②③④ B.⑤②④①
C.①③⑤②④① D.①③⑥⑤②④①
2、用氯化钠固体配制50 g质量分数5%的氯化钠溶液,下列仪器中需要用到的是( )
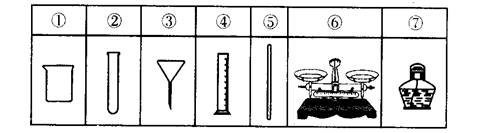
A.②④⑥⑦ B.①④⑤⑥
C.①③⑤⑦ D.①③④⑥
3、在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,量筒中有少量水残余
D.将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液
4、如图是A、B两种固体物质的溶解度曲线,下列说法中正确的是( )
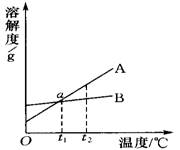
A.A物质的溶解度大于B物质的溶解度
B.t1℃时,a点表示A、B两种物质的溶解度相等
C.t2℃时,A、B两种物质的饱和溶液中溶质质量分数相等
D.A、B两种物质的饱和溶液各100g,由t2℃降到t1℃时析出的晶体一样多
5、下图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )
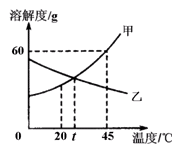
A. 甲物质的溶解度为60g
B. t℃时,甲、乙两物质的溶解度相等
C. 升高温度可使不饱和的甲溶液变为饱和
D. 乙物质的溶解度随温度的升高而增大
6、甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
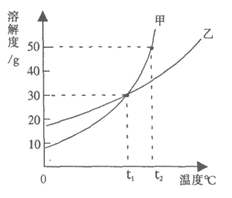
A. t1℃时,甲、乙各30g分别加入70g水中均能恰好完全溶解
B. t1℃时,甲和乙的饱和溶液中溶质的质量分数相等
C. t2℃时,在l00g水中放入60g甲,所得溶液溶质的质量分数为37.5%
D. t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
7、关于如图两种物质的溶解度曲线说法正确的是( )
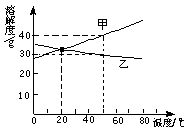
A. 升高温度,可使甲的不饱和溶液变为饱和溶液
B. 50℃时甲的饱和溶液溶质的质量分数为40%
C. 20℃时,甲、乙两种物质的溶解度相等
D. 要使乙从其浓溶液中析出,可冷却乙的热浓溶液
8、下图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
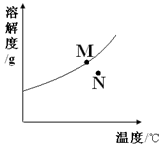
A. 从N→M:先向N中加入适量固体A再降温
B. 从N→M:先将N降温再加入适量固体A
C. 从M→N:先将M降温再将其升温
D. 从M→N:先将M升温再将其蒸发掉部分水
9、在实验室配制溶液时,常涉及以下过程:①溶解;②称量;③计算;④装瓶存放。请按要求回答问题:
(1)现欲配制50g 5%氯化钠溶液,配制过程的先后顺序是__________ (填序号)。
(2)用已调节平衡的天平称取氯化钠固体时,发现指针偏右,接下来的操作是____________________。
(3)在量取蒸馏水体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分数__________ (填“<”或“>”)5%。
(4)在溶解步骤中需要的仪器有__________、__________。
10、下图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图。
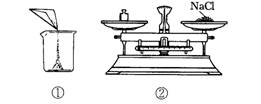
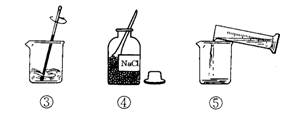
(1)配制过程中使用的四种玻璃仪器,分别是广口瓶、__________、__________、量筒。
(2)请你指出图中一处错误操作,并分析该操作可能造成的后果__________ ____________________。
(3)图②、图③表示的操作步骤分别是______________________________
(4)配制时需称量氯化钠__________g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数__________ (填“偏大”或“偏小”);量取水最好选择__________的量筒(填序号①10mL ②50mL ③100mL)(水的密度为1g/cm3)。
(5)下列错误操作可能导致溶液溶质质量分数小于12%的是(填序号) __________。
①B操作时食盐和砝码位置颠倒了
②A操作中有固体洒落
③用量筒量取蒸馏水时,仰视凹液面最低处读数
④E操作中有少量水洒出
⑤C操作中有溶液洒出