例1、(内蒙古包头)滴有酚酞试液的氢氧化钠溶液分别与下列物质混合后,溶液一定呈红色的是( )
A.硫酸镁溶液 B.氯化钠溶液
C.稀盐酸 D.二氧化碳
解析:
A项中MgSO4+2NaOH=Mg(OH)2↓+Na2SO4,反应后生成的Mg(OH)2是沉淀物,若NaOH不过量,溶液中不存在OH-,故溶液不一定呈红色;B项中NaOH与NaCl不反应,溶液中存在OH-,故溶液一定呈红色;C项中若稀盐酸与NaOH恰好完全中和或酸过量时,溶液便不呈红色;D项中二者反应生成的Na2CO3或NaHCO3溶液也呈碱性,不管NaOH溶液的量不足还是过量,溶液始终呈红色。
答案:BD
例2、(江苏常州)工业生产中,可用盐酸洗去铁材表白的致密氧化层,但冬天反应变缓而影响生产,为提高酸冼液的浓度或温度以加快反应,保证生产,可在酸洗液中加入( )
A.食盐 B.生石灰
C.浓硫酸 D.固体氢氧化钠
解析:
生石灰、浓硫酸、固体氢氧化钠溶于水都能使溶液的温度升高,但生石灰和氢氧化钠溶液能与盐酸反应,使酸洗液的浓度降低,故选C。
答案:C
例3、(山东潍坊)2008年诺贝尔化学奖授予发明和研究绿色荧光蛋白的三位科学家。绿色荧光蛋白分子中含有氨基(一NH2,具有碱的性质)和羧基(—COOH,具有酸的性质)。绿色荧光蛋白具有的性质是( )
A.既能与盐酸反应,又能与氢氧化钠反应
B.只能与氢氧化钠反应,不能与盐酸反应
C.只能与盐酸反应,不能与氢氧化钠反应
D.既不能与盐酸反应,又不能与氢氧化钠反应
解析:
依据题中材料可知:氨基具有碱的性质,羧基具有酸的性质,因此绿色萤光蛋白分子既有酸的性质(能与碱反应),又具有碱的性质(能与酸反应)。
答案:A
例4、(北碚实验区)(1)现有H+、OH-、NO3-、Fe3+四种离子,请写出它们可能组成的酸、碱、盐的化学式:酸________;碱_________;盐__________。
(2)根据表中示例填空:
类别 |
物质 |
化学性质(方程式) |
用途 |
酸 |
稀硫酸 |
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O |
金属制品的除锈 |
碱 |
氢氧化钙溶液 |
|
|
氢氧化铝固体 |
|
治疗胃酸过多 |
盐 |
碳酸钙固体 |
|
|
答案:
(1)HNO3;Fe(OH)3;Fe(NO3)3
(2)Ca(OH)2+CO2=CaCO3↓+H2O;检验CO2气体;
2A1(OH)3+6HCl=2A1Cl3+3H2O ;
CaCO3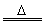 CaO+CO2↑;制生石灰
CaO+CO2↑;制生石灰
解析:
本题主要考查酸、碱、盐的概念、组成、化学性质及用途。(1)一般情况下,酸由H+和酸根离子构成,一定含有H元素;碱由OH-和金属离子构成,一定含有H、O两种元素;盐由金属离子(或NH4+)和酸根离子构成,一定含有非金属元素,掌握上述知识,结合题给离子不难写出酸、碱、盐的化学式。(2)本小题第1空具有开放性,Ca(OH)2溶液还可以与Na2CO3溶液反应制取NaOH。
例5、选择适当试剂除去括号中的杂质(用化学方程式表示)。
(1)HNO3(HCl)_____________; (2)HCl(H2SO4)_____________。
解析:
除杂质需注意两点:一是所选试剂必与杂质反应,二是不能引入新的杂质。
解答:
(1)HCl+AgNO3=AgCl↓+HNO3
(2)H2SO4+BaCl2=BaSO4↓+2HCl