(一)构成物质的微粒
1、分子和原子
| |
分子 |
原子 |
定义 |
分子是保持物质化学性质最小的微粒 |
原子是化学变化中的最小微粒。 |
性质 |
(1)分子很小(体积小、质量小)
(2)分子是在不断运动的
(3)分子间有间隙
(4)同种分子性质相同,不同种分子性质不同 |
(1)原子很小(体积小、质量小)
(2)原子是在不断运动的
(3)原子间有间隙 |
联系 |
分子是由原子构成的。分子、原子都是构成物质的微粒。 |
区别 |
化学变化中,分子可分,原子不可分。 |
(1)化学变化的实质:在化学变化中,分子分裂成原子,原子重新结合成新的分子。
(2)分子构成的描述:分子是由原子构成。如:
单原子分子:如稀有气体的分子只是1个原子 (如:He)
双原子分子:由2个原子构成的分子(如:H2、O2、N2、HCl等)
多原子分子:由2个以上的原子构成的分子 (如H2O为三原了分子,NH3为四原子分子)
2、原子的构成
(1)原子结构

(2)原子结构示意图
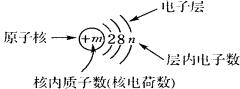
①m决定元素种类;
②n与元素的化学性质关系密切;
③m=2+8+n;
④在化学反应中,n可变,m不可变。
(3)原子中:核电荷数=质子数=核外电子数=原子序数
(4)原子核内质子数不一定等于中子数,如普通氢原子核内无中子。
(5)原子的质量主要集中在原子核上,近似相对原子质量=质子数+中子数
3、离子
(1)定义:带电荷的原子(或原子团)叫做离子,如Na+、Cl-、SO42-等。
(2)离子的分类
阳离子:带正电荷的原子(或原子团),如Na+、Mg2+、NH4+
阴离子:带负电荷的原子(或原子团),如Cl-、S2-、SO42-
(3)离子的形成:金属原子一般失电子形成阳离子;非金属原子一般得电子形成阴离子。
(4)书写:在元素符号或原子团的右上角标上离子所带电荷,数目在前,正负号在后。离子带1个单位正电荷或1个单位负电荷时,“1”省略不写。如Na+、Cl-、Mg2+、S2-、SO42-等。
(5)原子和离子的比较
粒子种类 |
原子 |
离子 |
阳离子 |
阴离子 |
区别 |
粒子结构 |
质子数=核外电子数 |
质子数>核外电子数 |
质子数<核外电子数 |
粒子电性 |
中性 |
正电 |
负电 |
联系 |

|
(二)物质的组成元素和分类
1、概念:元素是具有相同核电荷数(即核内质子数)的一类原子的总称。“一类原子”包括:
(1)质子数相同、中子数不同的原子,如Cl-35、Cl-37两种原子都属于氯元素;
(2)质子数相同的不同化合价的元素,如0、+1、+3、+5、+7、-1价的氯元素;
(3)质子数相同的单核离子,如Cl-属于氯元素。
2、分类:(1)金属元素;(2)非金属元素;(3)稀有气体元素。(元素的中文名称的偏旁可看出)
3、地壳中含量列前四位的元素是:氧、硅、铝、铁。
4、生物细胞中含量列前四位的元素是:氧、碳、氢、氮。
(三)分子、原子、离子、元素的关系
元素是物质的宏观组成,原子、分子、离子是物质的微观组成。
分子:一部分单质和化合物是由分子构成的,如氢气(H2)、氧气(O2)、水(H2O)等。
原子:金刚石等固体非金属(有例外,如碘)、金属、稀有气体是由原子直接构成的。
离子:离子化合物均由离子构成,如氯化钠,典型的金属元素(如Na、Mg等)与典型的非金属元素(如F、O、Cl、S等)形成的化合物均是离子化合物。
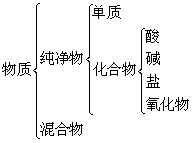
(四)物质的分类
1、科学家设想宇宙中可能存在完全由反粒子构成的物质――反物质;物质与反物质相遇会释放出巨大的能量,在能源研究领域中前景可观。正电子、负质子等都是反粒子,它们跟通常听说的电子、质子相比较,质量相等但电性相反。请你推测,反氢原子的结构可能是( )
A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成
解析:
氢原子由1个带正电荷的质子和1个带负电荷的电子构成,那么,反氢原子由1个带负电荷的质子和1个带正电荷的电子构成。
答案:B
2、用分子的观点解释下列现象,正确的是( )
A.热胀冷缩是因为分子大小随温度而改变;破镜不能重圆说明分子间有间隔
B.蔗糖能溶于水说明分子做无规则运动;食物腐败说明分子发生了变化
C.气体易被压缩说明分子间间隔很小;花香四溢说明分子做无规则运动
D.石灰石能被粉碎成粉末说明分子很小;酒精挥发说明分子间间隔变大
解析:
热胀冷缩是因为分子间间隔随温度而改变;气体易被压缩说明分子间有间隔;石灰石能被粉碎成粉末说明分子间有间隔;其他都是正确的。
答案:B
3、物质都是由微粒构成的,下列物质由分子构成的是( )
A.干冰 B.碳酸钠
C.金刚石 D.铜
解析:
干冰是由分子构成的;碳酸钠是由离子构成的;金刚石是由原子构成;铜是由原子构成。
答案:A
4、我国的“神舟五号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的氦(He-3)。其原子核中质子数为2、中子数为1,每百吨氦(He-3)核聚变所释放出的能量相当于目前人类一年消耗的能量。下列关于氦(He-3)元素的说法正确的是( )
A.原子核外电子数为3 B.相对原子质量为2
C.原子结构示意图为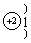 D.原子结构示意图为
D.原子结构示意图为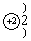
解析:
原子核外电子数为等于质子数,应为2;相对原子质量等于质子数和中子数的和,应为2+1=3。
答案:D
5、下列各组物质,按化合物、混合物顺序排列的是( )
A.食盐、干冰 B.胆矾、石灰水
C.红磷、烧碱 D.水银、生理盐水
解析:
干冰、胆矾、烧碱是化合物,食盐、石灰水、生理盐水是混合物,红磷、水银是单质。
答案:B
6、下图是表示气体微粒的示意图,图中“●”和“○”分别表示不同的原子,其中表示纯净物的是( )
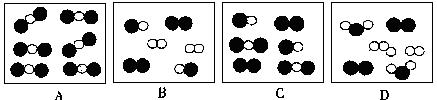
解析:
看微粒的示意图里有几种分子。只有一种分子的是纯净物。
答案:A
7、20世纪20年代,就有人预言可能存在由4个氧原子构成的氧分子(O4),但一直没有得到证实。最近,意大利的科学家使用普通氧分子和带正电的氧离子制造出了这种新型氧分子,并用质谱仪探测到了它的存在。下列叙述中正确的是( )
A.O4是一种新型的化合物
B.一个O4分子中含有2个O2分子
C.O4和O2的性质完全相同
D. O4和O2混合后形成的是混合物
解析:
O4和O2是同种元素组成的不同物质。
答案:D