(一)金属材料
1、金属材料:纯金属和合金
2、合金:一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质。(属于混合物)
3、金属的物理性质:
(1)常温下一般为固态(汞为液态),有金属光泽。
(2)大多数呈银白色(铜为紫红色,金为黄色)
(3)有良好的导热性、导电性、延展性
4、合金的优点:一般说来,合金的颜色比各成分的颜色鲜艳;熔点比各成分低;硬度比各成分大;抗腐蚀性能更好。
(二)金属的化学性质
常见金属活动性顺序:

1、大多数金属可与氧气反应
2、金属+酸→盐+氢气
①在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
②金属与浓硫酸、硝酸反应不生成氢气;
注意:金属越活泼,与酸反应生成氢气的速率越快。
3、金属+盐→另一金属+另一盐
①在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来。
②K、Ca、Na除外(K、Ca、Na能与盐溶液中的水反应)
③盐必须是可溶性盐
(三)置换反应
1、置换反应:一种单质跟一种化合物反应,生成另一种单质和另一种化合物的反应。
2、类型
(1)金属置换出非金属,如
①金属和酸反应:Zn+H2SO4=ZnSO4+H2↑ ②特例:2Mg+CO2 2MgO+C
2MgO+C
(2)金属置换出金属,如
金属和盐溶液反应:Fe+CuSO4=FeSO4+Cu;Cu+2AgNO3=Cu(NO3)2+2Ag
(3)非金属置换出金属,如
碳(或氢气)还原金属氧化物:C+2CuO 2Cu+CO2↑;H2+CuO
2Cu+CO2↑;H2+CuO Cu+H2O
Cu+H2O
(4)非金属置换出非金属,如:C+H2O CO+H2
CO+H2
(四)金属活动性顺序的应用
1、金属和酸反应的图形
(1)金属和酸反应生成氢气的快慢:金属越活泼,与酸反应生成氢气的速率越快
(2)金属和酸反应生成氢气的多少(以+2价的金属为例)
①相同质量的两种金属分别和足量的相同质量的酸反应(两种金属都会反应完),相对原子质量小的金属生成的氢气多。
②相同质量的两种金属分别和适量的相同质量的酸反应,一种金属反应完,另一种金属剩余(相对原子质量小的金属会剩余),相对原子质量小的金属生成的氢气多。
③相同质量的两种金属分别和少量的相同质量的酸反应(两种金属都会剩余),两种金属生成的氢气一样多。
2、金属和盐溶液反应
(1)一种金属和一种盐溶液反应的分析
(2)一种金属和两种盐溶液反应的分析
3、金属活泼性的判断依据
(1)金属在自然界的存在
(2)金属对应碱的溶解性
(3)金属和酸反应的速度
(4)置换反应:A+BC→AC+B 能否发生
4、探究金属活泼性方案的设计
(1)设计实验看置换反应:A+BC→AC+B 能否发生
(2)设计实验:将金属放入酸中,比较放出气泡的速率
1、2005年7月,美国“深度撞击”飞行器成功炮轰彗星,其撞击器采用的是一种含铍(一种金属)3%的铜合金。关于合金,下列说法错误的是( )
A.合金属于金属材料
B.只能由金属熔合而成
C.合金比纯金属性能更优
D.生铁和钢都是铁的合金
解析:
合金是一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质。
答案:B
2、下列物质可以由金属与酸直接发生置换反应制得的是( )
A.硫酸铁 B.氯化铜
C.硫酸锌 D.硝酸镁
解析:
要注意金属与酸直接发生置换反应的特点。反应;Zn + H2SO4=ZnSO4+H2↑可以实现。
答案:C
3、下列事实不能说明Zn比Ag活泼的是( )
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420℃,Ag的熔点为962℃
解析:
金属活泼性的判断依据:(1)金属在自然界的存在;(2)金属对应碱的溶解性;(3)金属和酸反应的速度;(4)置换反应:A+BC→AC+B 能否发生。
答案:D
4、将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价) ( )
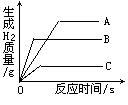
A.放出H2的质量是A>B>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
解析:
(1)金属和酸反应生成氢气的快慢:金属越活泼,与酸反应生成氢气的速率越快
(2)金属和酸反应生成氢气的多少(以+2价的金属为例):相同质量的金属分别和足量的相同质量的酸反应(金属都会反应完),相对原子质量小的金属生成的氢气多。
答案:AD
5、将过量铁粉投入盛有硫酸铜和硫酸锌混合溶液的烧杯中,充分反应后,过滤,留在滤纸上的物质是( )。
A.Zn、Cu和Fe B.Cu
C.Zn和Cu D.Cu和Fe
解析:
铁和硫酸铜可以反应,铁和硫酸锌不反应。
答案:D
6、要探究锌、铜、银三种金属的活动性顺序,不能选用下列哪组试剂进行实验( )
A.Zn、CuSO4、Ag B.Zn、Cu、AgNO3
C.Zn、Cu、H2SO4 D.ZnSO4、Cu、AgNO3
解析:
Zn和H2SO4能反应,而Cu和H2SO4不能反应,说明Zn比Cu活泼。但无法比较锌、铜、银三种金属的活动性顺序。
答案:C
7、取某铁样品6 g与足量的稀盐酸反应,生成0.2 g氢气.则该铁的样品中可能含有的杂质是( )
A.镁 B.铜
C.锌 D.铝
解析:
若纯铁与足量的稀盐酸反应,生成0.2 g氢气,则需要纯铁5.6g。而现在铁样品6 g与足量的稀盐酸反应,生成0.2 g氢气,说明样品中含有的杂质比相同质量的铁与盐酸反应生成的氢气少,符合条件的有铜和锌。
答案:BC
8、下列反应不属于置换反应的是( )
A.Fe+CuSO4=Cu+FeSO4
B.3CO + Fe2O3 2Fe+3CO2
2Fe+3CO2
C.2F2+2H2O=O2+4HF
D.2KClO3+I2=2KIO3+C12
解析:
置换反应是一种单质跟一种化合物反应,生成另一种化合物的反应。B中两种反应物都是化合物,不是置换反应,该反应是非基本反应类型。
答案:B