例1、(江苏南京)下列各组离子在溶液中一定能大量共存的是( )
A.H+、Cl-、OH-
B.H+、SO42-、HCO3-
C.Ba2+、H+、SO42-
D.Cu2+、Cl-、NO3-
解析:
离子之间能相互反应,则离子不能共存。A中H+与OH-反应生成水;B中H+与HCO3-反应生成CO2和H2O;C中Ba2+与SO42-反应生成BaSO4沉淀。
答案:D
例2、(河南)人的胃液里含有适量盐酸。服用含MgCO3的抗酸药可治疗胃酸过多症,有关反应的化学方程式为____________;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用的优点是_______________。
答案:
MgCO3+2HCI=MgCl2+CO2↑+H2O; 药物与胃酸的接触面积大,反应快。
解析:
用含碳酸镁的药物把胃酸中过量的盐酸反应掉,以达到治疗目的;反应物接触面积越大,反应速率越快,“嚼食”的目的就是为了增大药物与胃酸的接触面积,使反应速率加快。
例3、(大连市)现有下列试剂:①石灰水 ②食醋 ③食盐水 ④纯碱溶液 ⑤烧碱溶液,其中,检验贝壳的主要成分为碳酸盐必须用到的是( )
A.②⑤ B.①② C.②④ D.①③
解析:
主要考查碳酸盐的检验方法。检验碳酸盐的主要方法是先向所给物质中滴加酸液,然后将产生的气体通入石灰水,观察现象,若澄清的石灰水变浑,则证明该物质是碳酸盐。分析题给试剂,要检验贝壳的主要成分是碳酸盐,应选择的试剂是①②。
答案:B
例4、(吉林省)下列各组物质中。分别加入稀盐酸后,会出现两种不同现象的是( )
A.Na2CO3和K2CO3 B.AgCl和BaSO4
C.Ba(NO3)2溶液和NaOH溶液 D.Fe和Zn
解析:
A组物质是两种白色粉末的碳酸盐,均能和盐酸反应产生无色气体和无色溶液;B组物质是不溶于稀硝酸的白色固体AgCl和BaSO4,盐酸不与它们反应;C组物质是两种无色溶液,盐酸只和其中的NaOH溶液发生中和反应,但没有任何现象;D组物质为Fe和Zn,盐酸和它们反应分别生成浅绿色的FeCl2溶液和无色的ZnSO4溶液,呈现出了两种不同的现象,故符合题意。
答案:D
例5、(黑龙江)某同学设计了四种物质制备的实验方案,其中理论上正确、操作上可行的是( )
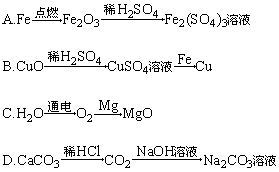
解析:
A项中铁燃烧生成Fe3O4,故其原理不正确,C项中由H2O电解制取O2,浪费能源,经济上不划算。
答案:BD