|
一周强化
一、一周知识概述
在本周,我们学习了第十一单位课题一“生活中常见的盐”。本课题要求我们做到以下几点:
1、了解氯化钠、碳酸钠、碳酸氢钠和碳酸钙的组成及其在生活中的主要用途。
2、能根据复分解反应发生的条件判断酸、碱、盐之间的反应能否发生。
3、掌握碳酸根离子的检验方法。
4、学习溶解、过滤、蒸发等实验操作技能,并综合运用相关操作、分离、提纯固体混合物。
二、重点知识归纳与讲解
1、几种常见的盐
下表是几种常见的盐的组成及主要用途。
名称 |
化学式 |
俗名 |
主要用途 |
氯化钠 |
NaCl |
食盐 |
作调味品,腌制食品;能维持人体正常生理机能;医疗上用来配制0.9%的生理盐水;工业上用NaCl做原料制NaOH、Cl2、盐等;农业上用NaCl溶液来选种 |
碳酸钠 |
Na2CO3 |
纯碱、苏打 |
用于生产玻璃、造纸、纺织、洗涤剂 |
碳酸氢钠 |
NaHCO3 |
小苏打 |
发酵粉的主要成分;治疗胃酸过多 |
碳酸钙 |
CaCO3 |
石灰石、大理石的主要成分 |
可用作补钙剂;做建筑材料;也可用于实验室、工业制二氧化碳 |
2、粗盐提纯
粗盐中含有较多的可溶性杂质和不溶性杂质,可通过溶解、过滤、蒸发、结晶的步骤来制取精盐。
3、盐的化学性质
盐的
性质 |
发生反应的条件 |
反应实例 |
反应
类型 |
与金属反应 |
金属活动性顺序表中排在前面的金属能把排在后面的金属从它的盐溶液中置换出来 |
Cu+2AgNO3=Cu(NO3)2+2Ag |
置换反应 |
与酸反应 |
符合复分解反应发生的条件且盐能溶于酸 |
CaCO3+2HCl=CaCl2+H2O+CO2↑ |
复分解反应 |
与碱反应 |
符合复分解反应发生的条件且盐、碱都能溶于水 |
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
复分解反应 |
与盐反应 |
符合复分解反应发生的条件且盐都能溶于水 |
Na2CO3+BaCl2=BaCO3↓+2NaCl |
复分解反应 |
三、难点知识剖析
1、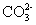 的检验 的检验
所用试剂:稀盐酸、澄清的石灰水。
现象:向样品中加入稀盐酸,有大量气泡产生,将生成的气体通入澄清石灰水,石灰水变浑浊。
2、复分解反应及其条件
(1)复分解反应:
两种化合物相互交换成分生成另外两种化合物。特点是:双交换,价不变。
(2)复分解反应发生的条件:
两种物质交换成分后,如果生成物中有沉淀或有气体或有水生成,则复分解反应就可以发生。
而对于碱与盐,盐与盐的反应,还要求反应物是可溶的。
(3)常见的复分解反应的归纳表:
反应物→生成物 |
复分解反应的实例 |
酸+金属氧化物→盐+水 |
Fe2O3+6HCl=2FeCl3+3H2O` |
酸+盐→新酸+新盐 |
Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
酸+碱→盐+水 |
HCl+NaOH=NaCl+H2O |
碱+盐→新碱+新盐 |
3NaOH+FeCl3=Fe(OH)3↓+3NaCl |
盐+盐→新盐+新盐 |
AgNO3+KCl=AgCl↓+KNO3 |
- 返回 -
|