例1、(2004・大连)为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化成氨气(化学式:NH3),再用稀硫酸吸收氨气,反应的化学方程式为:
2NH3+H2SO4=(NH4)2SO4
现取该牛奶样品30mL用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
(1)产生氨气的质量是多少克?(计算结果精确到0.01g,下同)
(2)30mL牛奶中含氮元素的质量是多少克?
(3)图中是该牛奶包装标签的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶样品中蛋白质的含量是否达到了包装标签所标示的蛋白质的质量标准。
解析:
本题主要涉及两类计算:一是根据化学方程式计算,二是根据化学式计算。
(1)设生产氨气的质量为x。
2NH3+H2SO4=(NH4)2SO4
2×17 98
x 9.5g×4.9%
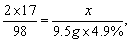
解得x≈0.16g
故产生氨气的质量为0.16g。
(2)氨气中氮元素的质量分数为: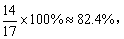
故30mL牛奶中氮元素的质量为:0.16g×82.4%≈0.13g。
(3)30mL牛奶中含蛋白质的质量为:0.13g÷16%≈0.81g。
故100mL牛奶中含蛋白质的质量为: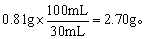
因为2.70g<2.90g,所以蛋白质的含量没有达到质量标准。
例2、(2004・安徽)今年春季,我省阜阳地区发生了震惊全国的“毒奶粉”事件。劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质含量,导致食用这种奶粉的众多婴幼儿严惩营养不良乃至死亡。奶粉中蛋白质含量的国家标准为:每100g婴幼儿奶粉中含12g~25g。其测定方法是:奶粉经系列反应生成氨,由氨计算出氮,再由氮求出蛋白质的质量(蛋白质含氮按15%计算)。
今有一袋从农村市场查获没收的奶粉,取样品100g,反应后生成的NH3和7.5g 19.6%的稀硫酸恰好完全反应[2NH3+H2SO4=(NH4)2SO4],试通过计算判断这袋奶粉是否属于劣质奶粉。
解析:
奶粉中每100克含蛋白质12―25克,即12%~25%;通过计算,求得的含量在这一范围内为优质奶粉,若低于12%为不合格奶粉。
答案:
设生成NH3的质量为x
2NH3+H2SO4=(NH4)2SO4
34 98
x 7.5g×19.6%
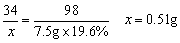
又设奶粉中蛋白质的质量分数为y
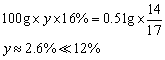
大大低于国家标准,属于劣质奶粉
例3、(2004・重庆北碚区)化学与人体健康密切相关,若人体血液缺铁,就会“贫血”;人体缺钙,会患佝偻病;缺碘会引起甲状腺肿大;缺氟易产生龋齿;缺锌会引起食欲不振等。
(1)市有“朴雪(补血)口服液”、“高钙牛奶”、“加碘食盐”、“加氟牙膏”、“葡萄糖酸锌”等商品,这些铁、钙、碘、氟、锌应理解为(填编号)_______。
(2)市售麦片中含有微量极细的还原铁粉,饮用这种麦片后,铁在胃液中变为亚铁盐的化学方程式为________。
(3)市售AD营养布丁的配料为:①蔗糖、②奶粉、③乳酸钙、④柠檬酸、⑤维生素、⑥维生素D、⑦食用色素、⑧食用香料、⑨防腐剂,其中属于营养素的有(填编号)________。
解析:
元素可理解为存在于单质和化合物中同一种原子的总称,故饮料、食品、药品、化肥商标上用元素符号标出的含量,高钙牛奶中的钙等均指元素。胃液中含有盐酸,铁在胃液中与盐酸反应生成亚铁盐。
答案:
(1)①。
(2)Fe+2HCl=FeCl2+H2↑
(3)①②③⑤⑥。