(一)单质、氧化物、酸、碱、盐的性质
1、金属
(1)大多数金属可与氧气反应生成金属氧化物
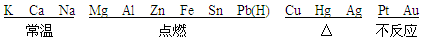
(2)金属+酸→盐+氢气
在金属活动性顺序里,位于氢前面的金属能置换出酸中的氢。
注意:①金属与浓硫酸、硝酸反应不生成氢气;
②金属越活泼,与酸反应生成氢气的速率越快。
(3)金属+盐→另一金属+另一盐
①在金属活动性顺序里,前面的金属能把后面的金属从它们的盐溶液中置换出来。
②K、Ca、Na除外(K、Ca、Na能与盐溶液中的水反应)
③盐必须是可溶性盐
2、氧化物
(1)金属氧化物
①金属氧化物+水→碱
生成的碱要可溶
②某些金属氧化物+酸→盐+水
这类金属氧化物属于碱性氧化物
(2)非金属氧化物
①非金属氧化物+水→酸
SiO2不发生此类反应,CO等也不与水反应
②某些非金属氧化物+碱→盐+水
这类金属氧化物属于酸性氧化物
3、酸
(1)与酸碱指示剂的反应:使紫色石蕊试液变红色,不能使无色酚酞试液变色
(2)金属+酸→盐+氢气
(3)某些金属氧化物+酸→盐+水
(4)碱+酸→盐+水
(5)盐+酸→另一种盐+另一种酸(产物符合复分解条件)
4、碱
(1)碱溶液与酸碱指示剂的反应:使紫色石蕊试液变蓝色,使无色酚酞试液变红色
(2)某些非金属氧化物+碱→盐+水
(3)酸+碱→盐+水
(4)可溶性碱+可溶性盐→另一种碱+另一种盐(产物符合复分解反应条件)
5、盐
(1)可溶性盐+金属1→金属2+新盐(金属1比金属2活泼,K、Ca、Na除外)
(2)盐+酸→新盐+新酸(满足复分解反应的条件)
(3)可溶性盐+可溶性碱→新盐+新碱(满足复分解反应的条件)
(4)可溶性盐+可溶性盐→两种新盐(满足复分解反应的条件)
(二)单质、氧化物、酸、碱、盐之间的转化
1、金属单质→金属氧化物→碱→盐
2、非金属单质→非金属氧化物→酸→盐
(三)物质的共存
1、几种物质或离子同存于一溶液的条件:相互间结合不能有沉淀或气体或水生成。
(1)Ag+与Cl-不能共存
(2)Ba2+与CO32-、SO42-不能共存
(3)H+与CO32-、OH-不能共存
(4)NH4+与OH-不能共存
(5)Ca2+与CO32-不能共存
(6)OH-与不Fe3+、Cu2+能共存
说明:溶液显酸性或pH<7;说明溶液中含有H+;
溶液显碱性或pH>7;说明溶液中含有OH-;
2、形成溶液的条件
几种物质溶于水形成溶液的条件:相互间不反应或反应不能有沉淀生成.做题时注意是否对溶液的颜色有要求.如无色;不能有Fe2+、Cu2+、Fe3+等
1、下列物质中,既不溶于水又不溶于盐酸,但能跟硝酸银溶液反应的是( )
A.Al B.CuO
C.BaSO4 D.Cu
解析:
将四个选项分别代入题干中进行检验,符合要求即可。
答案:D
2、下列各组内物质的转化不能一步实现的是( )
A.SO2→Na2SO3 B.BaCO3→BaCl2
C.CaCO3→CaO D.CuO→Cu(OH)2
解析:
A可通过SO2+2NaOH=Na2SO3+H2O实现;B可通过BaCO3+2HCl=BaCl2+H2O+CO2↑实现;C可通过CaCO3 CaO+CO2↑实现。
CaO+CO2↑实现。
答案:D
3、分别将下列各组物质同时加到水中,得到无色透明溶液的是( )
A.CuSO4、NaCl、KNO3
B.FeCl3、NaOH、MgCl2
C.Na2SO4、NaCl、BaCl2
D.NaOH、KCl、NaNO3
解析:
A中物质相互不反应且都可溶,可形成溶液,但CuSO4溶于水后溶液呈蓝色;B中FeCl3与NaOH、MgCl2与NaOH能反应生成Fe(OH)3、Mg(OH)2沉淀;C中Na2SO4与BaCl2可反应生成BaSO4沉淀; D中三种物质相互不反应且都可溶并呈无色。
答案:D
4、下列各组中的三种物质在同一溶液中能够大量共存的是( )
A.Na2CO3、HCl、NaNO3 B.NaCl、NaOH、MgCl2
C.KNO3、BaCl2、NaOH D.BaCl2、Na2SO4、KOH
解析:
A中,Na2CO3和HCl会反应;B中,NaOH和MgCl2会反应;D中,BaCl2和Na2SO4会反应。
答案:C
5、下列物质的水溶液,跟Ca(OH)2溶液、Fe2O3、Fe、AgNO3溶液都能反应的是( )
A.CuSO4 B.HCl
C.Na2CO3 D.HNO3
解析:
Ca(OH)2、Fe2O3、Fe、AgNO3这四种物质分别属于碱、碱性氧化物、金属单质、盐,那么能与这四种物质反应的物质应具有酸的通性,而HNO3与AgNO3不反应,所以符合条件的只有HCl。
答案:B
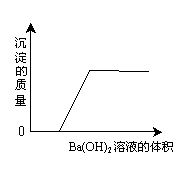
6、有一混合溶液是由盐酸、碳酸钠、硝酸钾、硫酸和氯化铜中的两种溶液混合而成。向该混合溶液中滴加氢氧化钡溶液,溶液体积的变化与生成沉淀质量的关系如下图所示,那么这两种溶液是( )

A.盐酸、硫酸 B.碳酸钠、硝酸钾
C.硝酸钾、盐酸 D.盐酸、氯化铜
解析:
从图象可看出,开始加入氢氧化钡没有产生沉淀。A中硫酸与氢氧化钡开始就会生成沉淀,不符合;B中碳酸钠与氢氧化钡开始就会生成沉淀,不符合;C中加入氢氧化钡不会产生沉淀,不符合;D中加入氢氧化钡先与盐酸反应,此时没有沉淀,当盐酸反应完时加入的氢氧化钡再与氯化铜反应产生沉淀,符合。
答案:D
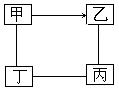
7、下图中“―”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为乙。下面四组选项中,符合下图要求的是( )
|
|
甲 |
乙 |
丙 |
丁 |
A |
H2SO4 |
NaOH |
NaCl |
Na2CO3 |
B |
CO |
CO2 |
H2SO4 |
CuO |
C |
Zn |
ZnSO4 |
Fe |
HCl |
D |
O2 |
CO |
CuO |
C |
解析:
A中H2SO4无法在一定条件下转化为NaOH;B中CO2和H2SO4不能在一定条件下反应;C中ZnSO4和Fe不能在一定条件下反应; D中O2和C反应生成CO,CO和CuO在加热时反应,CuO和C在高温时反应,C和O2在点燃时可反应,符合图形中的转化。
答案:D
8、以下表示的是碳及其化合物的相互转化关系:
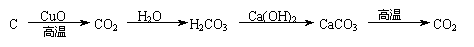
其中涉及的基本反应类型依次为( )
A.化合、置换、分解、复分解
B.置换、复分解、化合、分解
C.置换、化合、分解、复分解
D.置换、化合、复分解、分解
解析:
此转化中的反应分别为;C+2CuO 2Cu+CO2↑、H2O+CO2= H2CO3、
2Cu+CO2↑、H2O+CO2= H2CO3、
H2CO3+Ca(OH)2=CaCO3↓+2H2O、CaCO3 CaO+CO2↑,其反应类型依次为:置换、化合、复分解、分解。
CaO+CO2↑,其反应类型依次为:置换、化合、复分解、分解。
答案:D