注意
(1)在一般情况下,CO2既不能燃烧,也不能支持可燃物燃烧。但在一定条件下,某些物质也可以在CO2中燃烧,如点燃的镁条,伸入盛有CO2的集气瓶中能继续燃烧:
(2)CO2能溶解于水,通常1体积的水可以溶解1体积的CO2,增大压强时,还会溶解得更多些。CO2溶于水的同时还与水发生反应,但水中溶解的CO2只有1%跟水结合成H2CO3,其余仍以分子形式溶解在水中。
(3)能使紫色石蕊试液变红色的是H2CO3,而不是CO2。
3、二氧化碳对生活和环境的影响
(1)用途:①用于灭火;②用作致冷剂,用来保存食品和用于人工降雨;
③作肥料,制纯碱、汽水等。
(2)影响:近几十年来,由于人类消耗的能源急剧增加,森林遭到破坏,大气中二氧化碳的含量不断上升,造成“温室效应”。
4、一氧化碳的物理性质
通常状况下,一氧化碳是一种无色、无味的气体,它的密度比空气的略小,难溶于水。
5、一氧化碳的化学性质
(1)可燃性: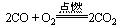 现象:燃烧时发出蓝色火焰,放出热量。
现象:燃烧时发出蓝色火焰,放出热量。
(2)还原性: 现象:黑色的氧化铜变红色,同时有使澄清的石灰水变浑浊的气体生成。
现象:黑色的氧化铜变红色,同时有使澄清的石灰水变浑浊的气体生成。