|
一周强化
一、周内容概述
在本周化学课的学习中,我们首先讲述了第八单元课题3金属资源的利用和保护,然后对第八单元进行了复习,通过对本单元的学习,我们应该知道本单元主要介绍了铁、铝、铜等重要金属和合金。涉及的范围较广,包括它们的性质,用途和资源保护等多方面的内容。要认真感受纯金属与合金的性质。金属与氧气、盐酸、稀硫酸、硝酸银等反应的不同。领悟物质的性质与物质用途的关系,认识到金属既有通性又有各自的特性。要注意对置换反应的理解,对金属活动性顺序,金属锈蚀条件的探究。知道怎样合理利用金属资源,保护金属资源,能进行有关杂质问题的计算。
二、重点知识归纳及讲解
(一)金属资源的利用和保护
1、常见的金属矿物
地球上的金属资源大多数以化合物的形式存在,只有少数很不活泼的金属如金、银等金属在自然界中有单质形式存在。化合态的金属在自然界中以矿物质形式存在。含有矿物的岩石称为矿石。下表列出了部分常见的金属矿物及主要成分。
矿物 |
赤铁矿 |
黄铁矿 |
菱铁矿 |
磁铁矿 |
赤铜矿 |
辉铜矿 |
黄铜矿 |
铝土矿 |
主要成分 |
Fe2O3 |
FeS2 |
FeCO3 |
Fe3O4 |
Cu2O |
Cu2S |
CuFeS2 |
Al2O3 |
2、铁的冶炼
将金属从它们的矿石中提炼出来的过程,叫做金属的冶炼。
|
生铁冶炼 |
原料 |
铁矿石、焦炭、石灰石、空气(氧气) |
原理 |
用还原剂在高温条件下将铁从矿石中还原出来 |
设备 |
高炉 |
高炉炼铁的反应方程式 |
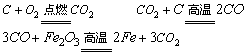
|
3、金属的腐蚀和防护
铁的锈蚀是铁与氧气和水直接接触,发生一系列化学反应,使铁转化为铁的化合物的过程。
(1)铁制品锈蚀的条件:
①要有能发生反应的物质(如氧气和水),反应物要能相互接触,②生成物不会对反应起阻碍作用。
铁锈的主要成分是Fe2O3・xH2O。铁锈太疏松,不能阻止里层的铁继续与氧气、水等反应,因此铁制品一旦生锈可以全部被锈蚀。
(2)防止铁制品锈蚀的方法:
保持铁制品表面的洁净干燥;在铁制品表面涂油脂或油漆,镀耐腐蚀的金属;在铁制品表面形成一层致密的氧化膜;在铁制品表面覆盖搪瓷、塑料;制成耐腐蚀的合金等。
4、金属资源保护
金属资源保护的途径:
(1)防止金属被腐蚀;
(2)回收利用废旧金属;
(3)合理、有计划地开采矿物;
(4)寻找金属代用品。
(二)第八单元知识框架归纳
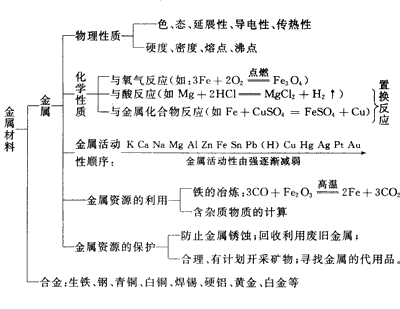
三、难点知识剖析
有关杂质问题的计算
化学方程式表示的是纯物质之间发生化学变化时的化学计算关系。根据化学方程式计算时,代入的量必须是纯物质的量。因此,当反应物含有杂质时,必须先把含杂质的物质的质量换算成纯物质的质量。计算公式:

- 返回 -
|