(一)海水所拥有的资源
1、海洋化学资源;
食盐、溴、镁、重水等。
2、海洋生物资源;
3、海底矿物资源;
4、海洋能源。
(二)海水中盐的开发和利用
1、海水制盐
(1)原理:利用日光、风力等
蒸发水,使溶于水中的食盐浓缩至饱和后析出。
(2)方法:蒸发法(盐田法)。
(3)盐田的结构及作用
①贮水池:引入海水静置,使泥沙沉降;
②蒸发池:利用日光、风力等自然蒸发作用使含盐水浓缩至接近饱和;
③结晶池:较浓含盐水继续浓缩,达到饱和后析出食盐晶体。
(4)优缺点:
节约燃料。但是,海水晒盐受天气限制,占用大量平坦土地,劳动条件十分艰苦,生产效率低。海水制盐中得到的是粗盐,粗盐中常含有Ca2+、Mg2+、(SO4)2-等杂质离子,必须精制提纯。
2、电解原理
(1)电解:使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程。
(2)电解池:把电能转变为化学能的装置,也叫电解槽。
①电极名称:
阳极:与电源正极相连的电极(或溶液中阴离子趋向的电极)
阴极:与电源负极相连的电极(或溶液中阳离子趋向的电极)
②电极反应:
阳极:氧化反应
阴极:还原反应
(3)电解过程
电解质电离产生的阴、阳离子在电流的作用下定向移动,阳离子在阴极得到电子,发生还原反应,阴离子在阳极失去电子,发生氧化反应,电子从电源负极沿导线流入阴极,从阳极流出,沿导线回到电源的正极,所以,电解质溶液的导电过程,就是该溶液的电解过程。
3、食盐资源的利用――氯碱工业
人们把以电解食盐水为基础制取氯气、烧碱(NaOH)等产品的工业称为“氯碱工业”。
(1)电解饱和食盐水制烧碱
通电前: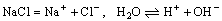 ,溶液中有Na+、Cl-、H+、OH-。
,溶液中有Na+、Cl-、H+、OH-。
通电时:Na+、H+趋向阴极,其中H+放电。
Cl-、OH-趋向阳极,其中Cl-放电。
电极反应式为:阴极:2H++2e-=H2↑
阳极:2Cl--2e-=Cl2↑
总反应为: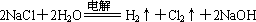
注意:
①NaOH在阴极区生成;
由于Na+、H+、Cl-、OH-四种离子中只有H+、Cl-放电,故在电解过程中c(Na+)在阳极、阴极区均近似相等,NaOH的生成只取决于c(OH-)的大小。OH-尽管趋向阳极,但由于在阳极上是Cl-放电,因此NaOH不是在阳极区生成,在阴极区,H+放电,促进了水的电离,水的电离平衡被破坏,致使c(OH-)>c(H+),故NaOH在阴极区生成。
②H2在阴极区生成,Cl2在阳极区生成。
不足:
①H2和Cl2混合不安全,易爆炸;
②Cl2会和NaOH反应,会使得到的NaOH不纯。
(2)离子交换膜法制烧碱
①离子交换膜电解槽的组成
由阳极(金属钛网)、阴极(碳钢网)、离子交换膜、电解槽框和导电铜棒等组成,每台电解槽由若干个单元槽串联或并联组成。下图表示一个单元槽的示意图。