1ЁЂМќЕФМЋадКЭЗжзгЕФМЋад
ЃЈ1ЃЉМЋадМќКЭЗЧМЋадМќ
ЁЁЁЁЂйИХФюЃКМЋадМќЪЧгЩВЛЭЌдзгМфаЮГЩЕФЙВМлМќЃЌЦфЙВгУЕчзгЖдЛсЗЂЩњЦЋвЦЁЃ
ЁЁЁЁЗЧМЋадМќЪЧгЩЭЌжждзгМфаЮГЩЕФЙВМлМќЃЌЦфЙВгУЕчзгЖдВЛЛсЗЂЩњЦЋвЦЁЃ
ЁЁЁЁЂкЬиеїЃКМЋадМќгаЕчадЕФе§ИКМЋЃЌдвђЪЧЙВгУЕчзгЖдгаЦЋЯђЃЛЗЧМЋадМќЮоЕчМЋадЃЌдвђЪЧЙВгУЕчзгЖдЮоЦЋЯђЁЃ
2ЁЂМЋадЗжзгКЭЗЧМЋадЗжзг
ЃЈ1ЃЉИХФю
ЁЁЁЁМЋадЗжзгЃКЗжзгжаМќЕФМЋадЕФЯђСПКЭВЛЕШгкСуЕФЗжзгЁЃ
ЁЁЁЁЗЧМЋадЗжзгЃКЗжзгжаИїМќЕФМЋадЕФЯђСПКЭЕШгкСуЕФЗжзгЁЃ
(2)ЗжзгМЋадЕФХаЖЯ
ЁЁЁЁaЃЎЫЋдзгЗжзгЕФМЋад
ЁЁЁЁВЛЭЌжждзгаЮГЩЕФЫЋдзгЗжзгЮЊМЋадЗжзгЁЃ
ЁЁЁЁЭЌжждзгаЮГЩЕФЫЋдзгЗжзгЮЊЗЧМЋадЗжзгЁЃ
ЁЁЁЁзмНсЃКЫЋдзгЗжзгжаЃЌМќЕФМЋадКЭЗжзгМЋадЪЧвЛжТЕФЃЌМДМќгаМЋадЗжзгОЭгаМЋадЃЛЗДжЎЃЌМќУЛгаМЋадЗжзгвВУЛгаМЋадЁЃ
ЁЁЁЁbЃЎЖрдзгЗжзгЕФМЋад
ЁЁЁЁЗЧМЋадМќЁЊЁЊЗЧМЋадЗжзгЁЃШчЃКP4ЁЃ
ЁЁЁЁМЋадМќЁЊЁЊЗЧМЋадЗжзгЁЃжБЯпаЭЗжзгЃЌШчCO2ЁЂBeCl2ЁЂC2H2ЃЛе§ЫФУцЬхаЭЗжзгЃЌШчCH4ЁЂCCl4ЃЛЦНУце§Ш§НЧаЮЗжзгЃЌШчBF3ЁЃ
ЁЁЁЁМЋадМќЁЊЁЊМЋадЗжзгЃЌШчH2OЁЂNH3ЕШЁЃ
ЁЁЁЁзмНсЃКХаЖЯABnаЭЗжзгМЋадгавЛОбщЙцТЩЃЌШєжааФдзгAЕФЛЏКЯМлЕФОјЖджЕЕШгкИУдЊЫиЫљдкЕФжїзхађЪ§ЃЌдђЮЊЗЧМЋадЗжзгЃЛШєВЛЕШЃЌдђЮЊМЋадЗжзгЃЌШчBF3ЁЂCO2ЕШЮЊЗЧМЋадЗжзгЃЛNH3ЁЂH2OЁЂSO2ЕШЮЊМЋадЗжзгЁЃ
ЃЈ3ЃЉЯрЫЦЯрШмдРэ
ЁЁЁЁЗЧМЋадШмжЪвЛАуФмШмгкЗЧМЋадШмМСЃЌМЋадШмжЪвЛАуФмШмгкМЋадШмМСЁЃ
2ЁЂЗЖЕТЛЊСІМАЦфЖдЮяжЪаджЪЕФгАЯь
ЁЁЁЁ(1)ИХФюЃКЗжзггыЗжзгжЎМфДцзХвЛжжАбЗжзгОлМЏдквЛЦ№ЕФзїгУСІНаЗжзгМфзїгУСІЃЌгжНаЗЖЕТЛЊСІЁЃ
ЁЁЁЁзЂвтЃКЂйЗжзгМфзїгУСІБШЛЏбЇМќШѕЕУЖрЃЌЫќжївЊгАЯьЮяжЪЕФШлЕуЁЂЗаЕуЁЂШмНтадЕШЮяРэаджЪЃЌЖјЛЏбЇМќжївЊгАЯьЮяжЪЕФЛЏбЇаджЪЁЃЂкдкРызгЛЏКЯЮяКЭН№ЪєОЇЬхжажЛДцдкЛЏбЇМќЁЃВЛДцдкЗжзгМфзїгУСІЃЌЗжзгМфзїгУСІжЛДцдкгкгЩЙВМлМќаЮГЩЕФЖрЪ§ЙВМлЛЏКЯЮяКЭОјДѓЖрЪ§ЗЧН№ЪєЕЅжЪЗжзгжЎМфЃЌМАЯЁгаЦјЬхЗжзгжЎМфЁЃЯёЖўбѕЛЏЙшЁЂН№ИеЪЏЕШгЩЙВМлМќаЮГЩЕФЮяжЪЕФЮЂСЃжЎМфВЛДцдкЗжзгМфзїгУСІЁЃЂлЗжзгМфзїгУСІЕФЗЖЮЇКмаЁ(вЛАуЪЧ300ЁЋ500pm)ЃЌМДЗжзгГфЗжНгНќ(ШчЙЬЬхКЭвКЬх)ЪБВХгаЯрЛЅМфЕФзїгУСІЁЃ
ЁЁЁЁЃЈ2ЃЉгАЯьЗЖЕТЛЊСІЕФвђЫи
ЁЁЁЁгАЯьЗЖЕТЛЊСІЕФвђЫижївЊАќРЈЃКЗжзгЕФДѓаЁЃЌЗжзгЕФПеМфЙЙаЭвдМАЗжзгжаЕчКЩЗжВМЪЧЗёОљдШЕШЁЃЖдзщГЩКЭНсЙЙЯрЫЦЕФЗжзгЃЌЦфЗЖЕТЛЊСІвЛАуЫцЯрЖдЗжзгжЪСПЕФдіДѓЖјдіДѓЁЃ
ЁЁЁЁЃЈ3ЃЉЗЖЕТЛЊСІЕФДѓаЁЖдЮяжЪЕФаджЪгаФФаЉгАЯьЃП
ЁЁЁЁД№ЃКЃЈ1ЃЉЖдЮяжЪШлЁЂЗаЕуЕФгАЯь
ЁЁЁЁвЛАуЫЕРДЃЌзщГЩКЭНсЙЙЯрЫЦЕФЮяжЪЃЌЯрЖдЗжзгжЪСПдНДѓЃЌЗжзгМфзїгУСІдНДѓЃЌЮяжЪЕФШлЗаЕуЭЈГЃдНИпЁЃШчШлЁЂЗаЕуЃК
ЁЁЁЁI2>Br2>Cl2>F2ЃЌRn>Xe>Kr>Ar>Ne>He
ЁЁЁЁЃЈ2ЃЉЖдЮяжЪШмНтадЕФгАЯь
ЁЁЁЁШчЃКдк273KЁЂ101kPaЪБЃЌбѕЦјдкЫЎжаЕФШмНтСП(0.049cm3ЁЄLЃ1)БШЕЊЦјдкЫЎжаЕФШмНтСП(0.024 cm3ЁЄLЃ1)ДѓЃЌОЭЪЧвђЮЊO2гыЫЎЗжзгжЎМфЕФзїгУСІБШN2гыЫЎЗжзгжЎМфЕФзїгУСІДѓЫљЕМжТЕФЁЃ
3ЁЂЧтМќМАЦфЖдЮяжЪаджЪЕФгАЯь
ЁЁЁЁЃЈ1ЃЉИХФюЃКЧтМќЪЧвЛжжМШПЩвдДцдкгкЗжзгжЎМфгжПЩвдДцдкгкЗжзгФкВПЕФзїгУСІЁЃЫќБШЛЏбЇМќШѕЃЌБШЗЖЕТЛЊСІЧПЁЃЕБЧтдзггыЕчИКадДѓЕФдзгXвдЙВМлМќНсКЯЪБЃЌHдзгФмЙЛИњСэвЛИіЕчИКадДѓЕФдзгYжЎМфаЮГЩЧтМќЁЃ
ЁЁЁЁЃЈ2ЃЉЬиеїЃКЧтМќЛљБОЩЯЛЙЪЧЪєОВЕчзїгУЃЌЫќМШгаЗНЯђадЃЌгжгаБЅКЭадЁЃ
ЁЁЁЁЃЈ3ЃЉБэЪОЗНЗЈЃКЭЈГЃгУXЁЊHЁYБэЪОЧтМќЃЌЦфжаXЁЊHБэЪОЧтдзгКЭXдзгвдЙВМлМќЯрНсКЯЁЃЧтМќЕФНЁГЄЪЧжИXКЭYЕФОрРыЃЌЧтМќЕФМќФмЪЧжИXЁЊHЁYЗжНтЮЊXЁЊHКЭYЫљашвЊЕФФмСПЁЃ
ЁЁЁЁЃЈ4ЃЉЧтМќЕФаЮГЩЬѕМў
ЁЁЁЁЂйЛЏКЯЮяжагаЧтдзгЃЌМДЧтдзгДІдкXЁЊHЁYЦфМфЁЃ
ЁЁЁЁЂкЧтжЛгаИњЕчИКадДѓЕФЃЌВЂЧвЦфдзгОпгазуЙЛаЁЕФдзгАыОЖЕФдЊЫиНсКЯКѓЃЌВХгаНЯЧПЕФЧтМќЃЌЯёетбљЕФдЊЫигаNЁЂOЁЂFЕШЁЃ
ЁЁЁЁЃЈ5ЃЉЧтМќЖдЮяжЪаджЪЕФгАЯь
ЁЁЁЁД№ЃКЂйЗжзгМфЧтМќЕФаЮГЩГ§ЪЙЮяжЪЕФШлЗаЕуЩ§ИпЃЌЖдЮяжЪЕФШмНтЖШЁЂгВЖШЕШвВЖМгагАЯьЁЃШчNH3МЋвзШмНтгкЫЎЃЌжївЊЪЧгЩгкАБЗжзгКЭЫЎЗжзгжЎМфаЮГЩСЫЧтМќЃЌБЫДЫЛЅЯрЕоКЯЃЌвђЖјМгДѓШмНтЁЃБљЕФгВЖШБШвЛАуЙЬЬхЙВМлЛЏКЯЮяЕФгВЖШДѓЃЌОЭЪЧвђЮЊБљжагаЧтМќНсЙЙЕФдЕЙЪЁЃ
ЁЁЁЁЂкЗжзгМфДцдкзХЧтМќЪБЃЌЦЦЛЕЗжзгМфЕФЧтМќЃЌЯћКФаэЖрЕФФмСПЃЌЫљвдДцдкзХЧтМќЕФЮяжЪОпгаНЯИпЕФШлЕуКЭЗаЕуЁЃ
ЁЁЁЁЂлЧтМќЕФДцдкЪЙЮяжЪЕФШмНтаддіДѓЁЃ
4ЁЂЪжад
(1)КЮЮЊЪжадЗжзгЃП
ЁЁЁЁД№ЃКШєвЛЖдЗжзгЃЌЫќУЧЕФзщГЩКЭдзгЕФХХСаЗНЪНЭъШЋЯрЭЌЃЌЕЋШчЭЌзѓЪжКЭгвЪжвЛбљЛЅЮЊОЕЯёЃЌдкШ§ЮЌПеМфВЛФмжиЕўЃЌетЖдЗжзгЛЅГЦЪжадвьЙЙЬхЁЃгаЪжадвьЙЙЬхЕФЗжзгГЦЮЊЪжадЗжзгЁЃ
(2)КЮЮЊЪжаддзгЃП
ЁЁЁЁД№ЃКЫФИіВЛЭЌЕФдзгЛђЛљЭХСЌНгдкдзгAЩЯЃЌаЮГЩЕФЛЏКЯЮяДцдкЪжадвьЙЙЬхЃЌдђAдзгОЭГЦЮЊЪжаддзгЁЃУПИіЪжаддзгЫљСЌНгЕФдзгЛђЛљЭХдкПеМфЕФХХВМОЭЯёзѓгвЪжЙиЯЕ(ЛђЪЕЮягыЦфОЕЯёЙиЯЕФЧбљЃЌЯрЫЦЕЋВЛФмжиЕў)
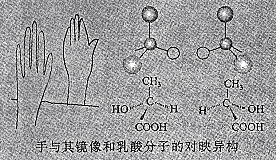
5ЁЂЮоЛњКЌбѕЫсЗжзгЕФЫсад
ЁЁЁЁКЌбѕЫсЕФЭЈЪНПЩаДГЩ(HO)mROnЃЌдђЮоЛњКЌбѕЫсЗжзгжаЗЧєЧЛљбѕЕФИіЪ§ЃЈМДnжЕЃЉдНЖрЃЌЦфЫсадОЭдНЧПЁЃР§ШчЃКЫсадЧПШѕHClO<HClO2<HClO3<HClO4ЁЃ
ЁЁЁЁР§1ЁЂЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈЁЁЃЉ
AЃЎЗжзгМфзїгУСІЪЧЗжзгМфЯрЛЅзїгУСІЕФзмГЦ
BЃЎЗжзгМфЧтМќЕФаЮГЩГ§ЪЙЮяжЪЕФШлЗаЕуЩ§ИпЃЌЖдЮяжЪЕФШмНтЖШЁЂгВЖШЕШвВЖМгагАЯь
CЃЎЗжзгМфзїгУСІгыЧтМќПЩЭЌЪБДцдкгкЗжзгжЎМф
DЃЎЧтМќЪЧвЛжжЬиЪтЛЏбЇМќЃЌЫќЙуЗКЕиДцдкгкздШЛНчжа
ЁЁЁЁНтЮіЃКЧтМќВЛЪЧЛЏбЇМќЃЌЛЏбЇМќЪЧдзггыдзгМфЧПСвЕФЯрЛЅзїгУЃЌЖјЧтМќЪЧЗжзгМфБШЗжзгМфзїгУСІЩдЧПЕФзїгУСІЃЌЫќУЧВЛЪЧАќКЌгыБЛАќКЌЕФЙиЯЕЁЃ
ЁЁЁЁД№АИЃКD
ЁЁЁЁЕуЦРЃКЗжзгМфзїгУСІКЭЧтМќЖМВЛЪЧЛЏбЇМќЃЌетСНепЖдЮяжЪЕФШлЗаЕуШмНтадЖМгаживЊгАЯьЁЃ
ЁЁЁЁР§2ЁЂЯТСаИїзщЗжзгжаЖМЪєгкКЌМЋадМќЕФЗЧМЋадЗжзгЕФЪЧЃЈЁЁЃЉ
AЃЎCO2ЁЂH2SЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЃЎC2H4ЁЂCH4
CЃЎCl2ЁЂC2H2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎNH3ЁЂHCl
ЁЁЁЁНтЮіЃКДЫЬтПМВщМќЕФМЋадКЭЗжзгЕФМЋадЁЃAжаCO2НсЙЙЮЊO=C=OЃЌH2SЮЊ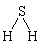 ЃЌЫљвдЖМКЌМЋадМќЃЌЕЋH2SЪЧМЋадЗжзгЃЛBжаC2H4ЮЊ
ЃЌЫљвдЖМКЌМЋадМќЃЌЕЋH2SЪЧМЋадЗжзгЃЛBжаC2H4ЮЊ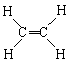 ЃЌCH4ЮЊ
ЃЌCH4ЮЊ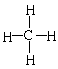 ЃЌЖМКЌМЋадМќЃЌЧвЖМЪєгкЗЧМЋадЗжзгЃЛCжаCl2ВЛКЌМЋадМќЃЌDжаNH3ЁЂHClЮЊМЋадЗжзгЃЌЖМВЛЗћКЯЬтвтЁЃ
ЃЌЖМКЌМЋадМќЃЌЧвЖМЪєгкЗЧМЋадЗжзгЃЛCжаCl2ВЛКЌМЋадМќЃЌDжаNH3ЁЂHClЮЊМЋадЗжзгЃЌЖМВЛЗћКЯЬтвтЁЃ
ЁЁЁЁД№АИЃКB
ЁЁЁЁЕуЦРЃККЌгаМЋадМќЕФЗжзгЪЧЗёгаМЋадашДгећИіЗжзгПДЁЃЗжзгРяЕчКЩЗжВМВЛЖдГЦдђЗжзгЮЊМЋадЗжзгЃЌШєећИіЗжзгРяЕчКЩЕФЗжВМЪЧЖдГЦЕФЃЌдђЗжзгЮЊЗЧМЋадЗжзгЁЃЫљвдЗжзгЕФМЋадгыЙЙГЩЕФЛЏбЇМќМАЗжзгЕФПеМфЙЙаЭгаЙиЯЕЁЃ
ЁЁЁЁР§3ЁЂЯТСаа№Ъіжае§ШЗЕФЪЧЃЈЁЁЃЉ
AЃЎвдЗЧМЋадМќНсКЯЦ№РДЕФЫЋдзгЗжзгвЛЖЈЪЧЗЧМЋадЗжзг
BЃЎвдМЋадМќНсКЯЦ№РДЕФЗжзгвЛЖЈЪЧМЋадЗжзг
CЃЎЗЧМЋадМќжЛДцдкгкЫЋдзгЕЅжЪЗжзгРя
DЃЎЗЧМЋадЗжзгжаЃЌвЛЖЈКЌгаЗЧМЋадЙВМлМќ
ЁЁЁЁНтЮіЃКЖдгкГщЯѓЕФбЁдёЬтПЩгУЗДР§ЗЈвдОпЬхЕФЮяжЪХаЖЯе§ЮѓЁЃAЪЧе§ШЗЕФЃЌШчO2ЁЂH2ЁЂN2ЕШЃЛBДэЮѓЃЌвдМЋадМќНсКЯЦ№РДЕФЗжзгВЛвЛЖЈЪЧМЋадЗжзгЃЌШєЗжзгЙЙаЭЖдГЦЃЌе§ИКЕчКЩжиаФжиКЯЃЌОЭЪЧЗЧМЋадЗжзгЃЌШчCH4ЁЂCO2ЁЂCCl4ЁЂCS2ЕШЃЛCДэЮѓЃЌЗЧМЋадМќвВДцдкгкФГаЉЙВМлЛЏКЯЮяжаЃЌШчH2O2ЁЂC2H4ЁЂC2H4ЁЂC2H5OHЕШКЭФГаЉРызгЛЏКЯЮяNa2O2жаЃЛDДэЮѓЃЌЗЧМЋадЗжзгжаВЛвЛЖЈКЌгаЗЧМЋадМќЃЌШчCH4ЁЂCO2ЁЃ
ЁЁЁЁД№АИЃКA
ЁЁЁЁР§4ЁЂЯТСаЮяжЪжаВЛДцдкЧтМќЕФЪЧЃЈЁЁЃЉ
AЃЎБљДзЫсжаДзЫсЗжзгжЎМф
BЃЎвКЬЌЗњЛЏЧтжаЗњЛЏЧтЗжзгжЎМф
CЃЎвЛЫЎКЯАБЗжзгжаЕФАБЗжзггыЫЎЗжзгжЎМф
DЃЎПЩШМБљ(CH4ЁЄ8H2O)жаМзЭщЗжзггыЫЎЗжзгжЎМф
ЁЁЁЁНтЮіЃКжЛгаЗЧН№ЪєадКмЧПЕФдЊЫигыЧтдЊЫиаЮГЩЧПМЋадЕФЙВМлМќжЎМфВХПЩФмаЮГЩЧтМќЃЌCЁЊHВЛЪЧЧПМЋадЙВМлМќЁЃЙЪбЁDЁЃ
ЁЁЁЁД№АИЃКD
ЁЁЁЁЕуЦРЃКзМШЗАбЮедкФФаЉЙВМлМќжЎМфФмаЮГЩЧтМќЁЃ