1、晶体与非晶体
(1)晶体的概念
具有规则的几何外形和固定熔点的固体是晶体。
①所谓规则的几何外形指的是晶体能自发地呈现多面体外形的性质。在宏观上,晶体和非晶体都可人工做成有规则几何外形的固体,但是在微观上,构成晶体的粒子在三维空间里呈周期性的有序排列,而非晶体则是构成微粒的无序排列。
②许多固体粉末用肉眼看不到晶体的外形,但在电子显微镜下可观察到规则的几何外形,这充分说明这些固体粉末也是晶体。
③由于晶体一般都具有固定的熔点,非晶体(大多是混合物)没有固定的熔点,所以我们可用有没有固定熔点来区分晶体和非晶体。
(2)晶体与非晶体的本质差异
| |
自范性 |
微观结构 |
晶体 |
有(能自发呈现多面体外形) |
原子在三维空间里呈周期性有序排列 |
非晶体 |
无 |
原子排列相对无序 |
(3)获得晶体的途径
①熔融态物质凝固
②气态物质凝华
③溶质从溶液中析出
2、晶胞
(1)定义:在晶体结构里,描述晶体结构的基本单元叫做晶胞。
(2)晶胞中粒子与晶胞的关系
晶胞只是晶体微观空间里的一个基本单元,在它的上、下、左、右、前、后无隙地排列着无数的晶胞,而且所有晶胞的形状及其内部原子的种类、个数、几何排列是完全相同的。因而,晶胞的顶角原子是被8个晶胞所共用的,晶胞棱上的原子是被4个晶胞所共用的,晶胞面上的原子是被两个晶胞所共用的,而只有位于晶胞的平行六面体内的原子才是完完全全被晶胞独自占有的。
(3)晶胞与晶体的关系
晶体是由无数肉眼看不见的,形状、大小、取向都相同的微小几何体(晶胞)“无隙并置”而成的。所谓“无隙并置”即一个晶胞与它的相邻晶胞是完全共顶角、共面、共棱的,取向一致,无间隙,从一个晶胞到另一个晶胞只需平移,不需转动,进行或不进行平移操作,整个晶体的微观结构不可区别。晶胞的这种本质属性可归纳为晶胞具有平移性。
例1、下图是玻璃的结构示意图,这张图说明玻璃是不是晶体?为什么?
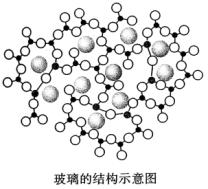
解析:晶体与非晶体的根本区别在于构成固体中的粒子在微观空间里是否呈现周期性的有序排列。观察玻璃的结构示意图,构成玻璃的粒子无周期性的排列,是无序的,所以玻璃是非晶体。
例2、举例说明有效鉴别真假宝石的方法?
答案:利用晶体与非晶体的性质差异来鉴别玻璃和宝石。宝石是晶体,具有固定的熔点和各向异性,可用硬度、熔点、折光率等性质来鉴别宝石。
(1)观察宝石的形状,具有多面体的外形;实验它的硬度,可在玻璃上划出痕迹,初步确定它是晶体;
(2)可利用宝石的折光率鉴别;
(3)可利用X-射线衍射仪鉴别。
例3、下图是铜晶胞示意图,请分析该晶胞中平均含有多少个铜原子?
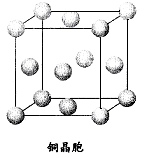
解析:一般晶胞都是平行六面体,晶体可以看作是晶胞在三维空间里共面堆积而成。每个晶胞的上、下、左、右、前、后共有六个与之共面的晶胞。处于晶胞顶点的粒子,同时为8个晶胞所共有,每个粒子只有1/8属于晶胞;处于棱上的粒子,同时为4个晶胞所共有,每个粒子只有1/4属于晶胞;处于面上的粒子,同时为两个晶胞所共有,每个粒子只有1/2属于晶胞;处于晶胞内部的粒子,则完全属于该晶胞。应用以上分摊法,便可确定铜晶体中平均所含的铜原子个数为:
顶点:8×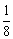
面心:6×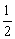
∴总数:8×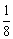 +6×
+6×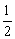 =4。
=4。
例4、下图是金属钠的晶胞示意图,算一算,它平均含有几个钠原子?
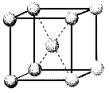
解析:应用分摊法可知金属钠晶胞中不同位置上平均分摊的钠原子数分别为:顶点:8×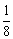 ,体心:1×
,体心:1×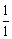 ,所以金属钠晶胞平均含有的钠原子个数为:8×
,所以金属钠晶胞平均含有的钠原子个数为:8×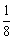 +1×
+1×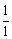 =2。
=2。