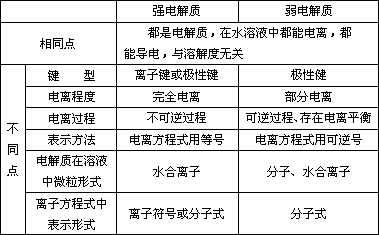
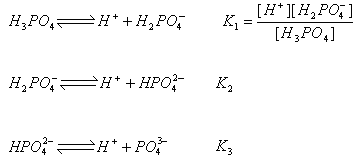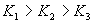(一)强电解质与弱电解质的比较
(二)弱电解质电离平衡的理解

勒夏特列原理不仅可用来判断化学平衡的移动方向,而且适用于一切动态平衡,当然也适用于电离平衡。与化学平衡一样,外界条件的改变也会引起移动。影响电离平衡的因素有:
①温度:电离是吸热的,故升高温度有利于电离;
②浓度:浓度越小,越有利于电离;
③同离子效应:加入与弱电解质具有相同离子的强电解质,能抑制电离;
(三)电离平衡常数的应用
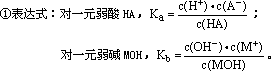
②K值越大,该弱电解质较易电离。在相同温度下,K值大小是比较弱电解质的电离程度和相对强弱的一个物理量。
③电离平衡常数同化学平衡常数一样,随温度的变化而变化。
④多元弱酸分步电离,每步都有电离常数