|
一周强化
一、一周知识概述
(一)、乙醇
1、乙醇的分子结构
分子式:C2H6O 结构式: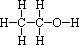
结构简式:CH3CH2OH或C2H5OH
官能团:―OH(羟基) 电子式: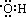
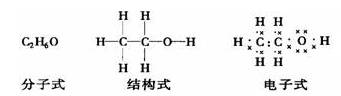
简写为CH3CH2OH或C2H5OH。 |

乙醇分子的比例模型 |
说明:羟基与氢氧根离子的比较
(1)电子式不同,羟基电子式为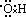 ;氢氧根离子电子式为 ;氢氧根离子电子式为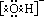 。 。
(2)羟基不显电性,氢氧根离子显电性;羟基不稳定,氢氧根离子较稳定。
(3)羟基不能独立存在,只能和别的“基”相结合在一起;氢氧根离子能独立存在,如OH-在溶液中或离子晶体中能独立存在。
2、乙醇的物理性质
(1)色、味、态:无色透明,具有特殊香味的液体。
(2)挥发性:易挥发
(3)溶解性:能与水以任意比互溶。
(4)沸点:78.5℃.
讨论:如何检验乙醇中是否含有水?
答案:常用无水CuSO4,若由白色变成蓝色说明存在水。
3、乙醇的用途
燃料、化工原料、有机溶剂、酿酒,70%~75%乙醇溶液可作消毒剂。
4、乙醇的化学性质
乙醇是非电解质,在溶液中不电离。官能团是羟基(―OH)。
(1)与活泼金属发生置换反应
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
(2)乙醇的氧化反应
①燃烧

现象:产生淡蓝色火焰,同时放出大量热。
用途:乙醇可作燃料。
②乙醇的催化氧化
在加热和有催化剂(Cu或Ag)存在的条件下,乙醇被氧化成乙醛。
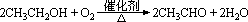
工业上利用此原理可生产乙醛。
思考: CH3OH和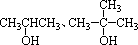 能否发生催化氧化? 能否发生催化氧化?
(3)乙醇的消去反应
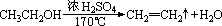 (此类消去反应又可称为分子内脱水反应) (此类消去反应又可称为分子内脱水反应)
思考: CH3OH和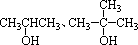 能否发生消去反应? 能否发生消去反应?
此外乙醇还有一种脱水反应称为分子间脱水反应,又可叫取代反应。
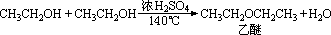
小结:乙醇的分子结构与化学性质的关系

(二)、醇类
1、醇的概念
醇是分子中含有跟链烃基直接相结合的羟基的化合物。
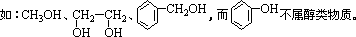
2、醇的分类
根据醇分子中羟基的数目:一元醇、二元醇、多元醇等。
根据醇分子中烃基是否饱和:
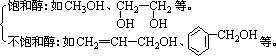
根据醇分子中是否含有苯环:
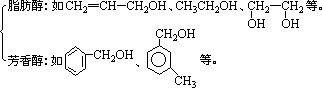
3、饱和一元醇分子式通式:CnH2n+2O(n≥1)
4、乙醇同系物物理性质
(1)溶解性:
甲醇、乙醇、丙醇可与水任意比互溶。分子中C4~C11醇,可部分溶于水,C12以上不溶于水。
(2)色态:低级为无色液体,其有特殊气味。
C4~C11为油状液体。
C12以上为无色无味蜡状固体。
5、化学通性
与乙醇相似,可与Na反应,可发生氧化反应、消去反应等。
说明:
(1)像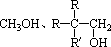 这样结构的醇不能发生消去反应,但可催化氧化。 这样结构的醇不能发生消去反应,但可催化氧化。
(2)像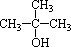 这样结构的醇不能催化氧化,但可发生消去反应。 这样结构的醇不能催化氧化,但可发生消去反应。
(3)像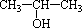 这样结构的醇催化氧化后不是醛类物质而是酮类物质 这样结构的醇催化氧化后不是醛类物质而是酮类物质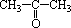 (丙酮)。 (丙酮)。
6、同分异构现象
由于碳链异构、官能团位置异构、不同类烃的衍生物(即类别异构)造成醇的同分异构现象普遍存在,如醇的类别异构可以是醚类物质(R―O―R′,其中R、R′为烃基),但在书写时,主要是要求能正确书写出醇类的同分异构体。
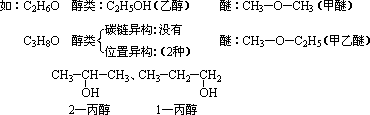
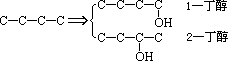
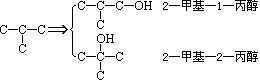
写出C4H10O属醇类的同分异构体。
书写思路是:先写碳链异构,再写位置异构。
7、几种重要醇
(1)甲醇:甲醇有毒,人饮用约10mL就能使眼睛失明,再多则能致死。
(2)乙二醇和丙三醇。
乙二醇和丙三醇都是无色、粘稠、有甜味的液体,乙二醇易溶于水和乙醇;丙三醇吸湿性强,能跟水、酒精以任意比混溶,它们都是重要的化工原料。此外,丙三醇还有护肤作用,俗称甘油。
二、重难点知识讲解
1、醇的催化氧化发生条件和规律
(1)发生条件:
醇分子结构中与―OH相连的碳原子上至少要有一个氢原子,即具有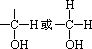 的结构。因为醇的催化氧化,其实质是“去氢”。 的结构。因为醇的催化氧化,其实质是“去氢”。
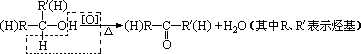
在有机反应中,氧化反应是指有机物去氢或加氧的反应。
上述氧化反应也可通过碳元素的平均价态的变化来理解。

(2)规律
①―OH连在链端点碳原子上的醇,即R―CH2OH结构的醇,被氧化成醛。
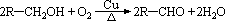
②与―OH相连碳原子上只有一个氢原子的醇,即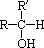 结构的醇,被氧化成酮( 结构的醇,被氧化成酮(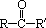 ,其中R、R′为烃基,可同,可不同)。 ,其中R、R′为烃基,可同,可不同)。
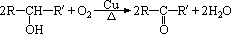
③与―OH相连碳原子上没有氢原子的醇,即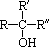 结构的醇(R、R′、R″为烃基,可相同可不同),不能被催化氧化。 结构的醇(R、R′、R″为烃基,可相同可不同),不能被催化氧化。
∵ 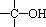 不能形成 不能形成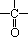 。 。
2、醇消去反应发生的条件
(1)醇分子结构:
与―OH相连的碳必须有相邻的碳原子,且此相邻的碳原子上还必须连有氢原子时,才能发生消去反应。
即: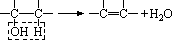
如: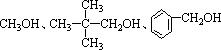 都不能发生消去反应。 都不能发生消去反应。
(2)反应条件:浓H2SO4,加热
- 返回 -
|