1、用铜锌合金制成假金元宝骗人的事件屡有发生。下列不易区别其真伪的方法是( )
A.测定密度
B.放入硝酸中
C.放入盐酸中
D.观察外观
2、下列各组离子在水溶液中能大量共存的是( )
A.H+、K+、NO3-、I-
B.SO42-、PO43-、K+、Na+
C.ClO-、Na+、K+、I-
D.PO43-、Cl-、Ba2+、Na+
3、下列对硝酸的认识不正确的是( )
A.打开浓硝酸的瓶盖会产生棕色的烟
B.锌跟稀硝酸的反应是置换反应
C.常用硝酸来制炸药、硫酸和化肥
D.稀硝酸也是一种强氧化性酸
4、将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),则所消耗的硝酸的物质的量是( )
A.0.12mol
B.0.11mol
C.0.09mol
D.0.08mol
5、对下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝罐来贮存,说明铝与浓硝酸不反应
D.反应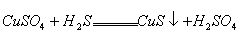 能进行,说明硫化铜既不溶于水,也不溶于稀硫酸
能进行,说明硫化铜既不溶于水,也不溶于稀硫酸
6、相同质量的四份铜片分别置于足量的下列酸中,所得到的气体的物质的量最多的是( )
A.浓硫酸
B.稀硫酸
C.浓硝酸
D.稀硝酸
7、实验室不需用棕色试剂瓶保存的试剂是( )
A.浓硝酸
B.硝酸银
C.氯水
D.浓硫酸
8、提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
9、从经济效益和环境保持考虑,大量制取硝酸铜最宜采用的方法是( )
A.Cu+HNO3(浓)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.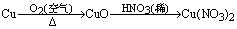
D.Cu+AgNO3→Cu(NO3)2
10、将硫化氢通入不同浓度的硝酸溶液中,发生下列反应:
① 3H2S+2HNO3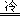 3S↓+2NO↑+4H2O
3S↓+2NO↑+4H2O
② H2S+2HNO3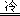 S↓+2NO2↑+2H2O
S↓+2NO2↑+2H2O
③ 4H2S+2HNO3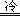 4S↓+NH4NO3+3H2O
4S↓+NH4NO3+3H2O
④ 5H2S+2HNO3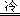 5S↓+N2↑+6H2O
5S↓+N2↑+6H2O
结合所学有关硝酸的知识,判断硝酸浓度由大到小的顺序,正确的是( )
A.①>②>③>④
B.②>①>④>③
C.②>①>③>④
D.④>③>②>①