1 、电极反应
分别在负极和正极进行的氧化和还原反应叫做电极反应。
负极 (-) Zn ,Zn-2e-= Zn2+(氧化反应)
正极 (+) Cu ,2H++2e-=H2↑(还原反应)
2 、电池反应
电极反应的总反应叫做总电池反应式或电池反应式,书写时,将两个电级反应式相加,消去电子,即得原电池的电池反应式。
电池反应式:Zn+2H+=Zn2++H2↑
如果把电池中的稀H2SO4换为醋酸溶液,电池反应式为:
Zn+2CH3COOH=(CH3COO)2Zn+H2↑
(三)、原电池的基本类型
1 、负极参与反应的原电池
这是最基本最早的原电池,例 Cu ― Zn 原电池(伏打电池)。
锌锰电池(干电池):锌皮是负极,中间碳棒是正极,石墨周围填充 ZnCl2 、 NH4Cl 和淀粉糊作电解液,填有 MnO2 吸收正极放出的 H2 ,电池反应式:
负极 (Zn) Zn-2e-=Zn2+
正极 (C) 2NH4++e-= 2NH3↑+H2↑
H2+MnO2=Mn2O3+H2O
正极产生的NH3被ZnCl2吸收:Zn2++4NH3=[Zn(NH3)4]2+
电池反应式:
2Zn+4NH4Cl+2MnO2=[Zn(NH3)4]Cl2+ZnCl2+Mn2O3+H2O
2 、两极都参加反应的原电池
可充电池都是两极都参加反应的原电池。这是一种发展较快较多的原电池,例铅蓄电池、锂电池、银锌电池(钮扣电池)、爱迪生蓄电池,它们的负极是较活的金属,正极是金属氧化物,放电时,负极被氧化,正极材料的金属氧化物被还原,充电时的电极反应与放电时相反。
【例】铅蓄电池,负极是Pb,正极板上有一层棕褐色PbO2,电池液是30%左右的H2SO4溶液。
铅蓄电池放电(工作)时的电极反应:
负极(Pb):Pb+SO42--2e-=PbSO4
正极(PbO2):PbO2+4H++2e-+SO42-=PbSO4+2H2O
电池反应式:
3 、两个电极都不参加反应的原电池
用惰性材料(如, Au 、 Pt 和石墨等)作电极(称为惰性电极)。电极本身不发生任何反应,而是引入两极上的适当物质发生氧化还原反应,如燃料电池,它是一种新兴的高能电池。应用于航天事业,它发展迅速、种类较多,负极通入可燃烧气体,如 H2 、 CH4 。它们燃烧时被氧化,正极通入氧化剂,如 O2 或空气,它们被还原,常用 KOH 或熔融 K2CO3 作电池液。
【例】由 H2 和 O2 构成的燃料电池,用 KOH 做电池液。
负极: H2+2OH--2e-=2H2O
正极: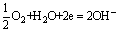
电池反应: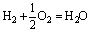
(四)、金属的腐蚀
金属的腐蚀是指金属或合金跟周围接触到的化学物质发生化学反应而腐蚀损耗的过程。
1 、实质
金属原子(M)失去电子而被氧化的过程,即M-ne-=Mn+。
2 、类型
有电化腐蚀和化学腐蚀两种。
(1) 电化腐蚀:不纯的金属 ( 或合金 ) 接触到电解质溶液发生原电池反应,相对较活泼的金属原子失去电子而被氧化所引起的腐蚀。
(2) 化学腐蚀:金属跟接触到的物质 ( 一般为非电解质 ) 直接发生氧化还原反应而引起的一种腐蚀。
负极:2Fe-4e-=2Fe2+
正极:2H2O+O2+4e-=4OH-
电化学腐蚀是造成钢铁腐蚀的主要原因 。
说明:①影响金属腐蚀的因素包括金属的本性和介质两个方面。就金属本性来说,金属越活泼,就越容易失去电子而被腐蚀。
介质对金属腐蚀的影响也很大,如果金属在潮湿的空气中,接触腐蚀性气体或电解质溶液,都容易被腐蚀。
②由于钢铁制品通常所处的外部环境干燥度较低,氧气的存在又非常广泛,在相同条件下,原电池反应比一般的氧化还原反应速率高,因此,在钢铁的腐蚀类型中主要是电化学腐蚀,其次是化学腐蚀。但是,钢铁的腐蚀类型并不单一,一般是电化学腐蚀与化学腐蚀并存,只是有主次之分而已。
③无论哪种类型的金属腐蚀,其本质都是金属被氧化。
4 、金属的防护方法
(1)改变金属的内部结构
如在铁中添加一些其它元素形成不锈钢,如镍铬不锈钢。
(2)覆盖保护层
(3)使用电化学保护法
① 外加电流的保护法
将被保护的金属与外加直流电源负极相连,能导电的惰性材料(如石墨)与电源正极相连,通电后,被保护的金属上积累电子而防止其被氧化而腐蚀。
② 外接活泼电极的保护法
在被保护的金属上连接一种更活泼的金属,当发生电化腐蚀时,首先锈蚀的是负极(活泼金属一极),这样就保护了另一极的金属不腐蚀。
此外,还有其它保护方法,这里不再介绍。
(五)、电极反应式的书写规律
1 、根据给出两个电极反应式,写总反应式
已知两个电极反应式,写总反应式并不难,只要使两个电极反应式得失电子数相等后,将两式相加,消去相同的化学式即可。
2 、给出总反应式,写出电极反应式
书写电板反应式的写法步骤一般分为四步:
(1)列物质、标得失;
(2)选离子、配电荷;
(3)配个数、巧用水;
(4)两式加、验总式。
3 、对于较复杂的原电池或电解池的过程,要分清什么发生了氧化反应,什么发生了还原反应,按照电荷守恒,写上 H+或 OH-或其它离子,考虑是否加 H2O ,最后通过两个反应相加来检验是否与题给总反应一致。