例1、目前上海大部分城市居民所使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
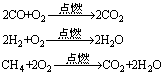
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是 ___________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是_____________。
管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:

试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是 __________________________。
解析:
由反应方程式可知,燃烧相同体积的管道气和天然气,天然气消耗 O2的体积大。因此,由管道煤气改烧天然气,就必须增大进氧气的量,以保证天然气充分燃烧,以防发生不完全燃烧生成CO,发生一氧化碳中毒。由表中数据知,丁烷沸点为-0.5℃,易液化。在寒冷的冬季,由于温度偏低使丁烷液化,导致管内气流不畅,出现火焰很小且呈断续状态。
答案:
天然气;增大;不能充分燃烧,生成有毒的 CO;丁烷遇冷凝结为液体使管道内气流不畅。
例2、利用天然气合成氨的工艺流程示意图如下:
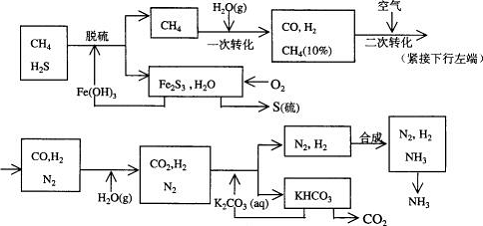
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是 ________________ 。
(2) n mol CH4 经一次转化后产生 CO 0.9n mol 、产生 H2__________ mol (用含 n 的代数式表示)。
(3) K2CO3 (aq)和 CO2 反应在加压下进行,加压的理论依据是 _________ (多选扣分)。
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由 KHCO3 分解得到的 CO2 可以用于 _______________ (写出 CO2 的一种重要用途)。
(5)整个流程有三处循环,一是 Fe(OH)3 循环,二是 K2CO3 (aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。
答案:(1)3H2S+2Fe(OH)3=Fe2S3+6H2O
(2)2.7n
(3)b
(4)生产纯碱(或作制冷剂等,其他合理答案也给分)

解析:
(1)流程图中已给出反应物是H2S和Fe(OH)3,生成物是Fe2S3和H2O,CH4没有参与反应,写出方程式再配平即可。
(2)写出此反应的方程:CH4+H2O→CO+3H2,很容易地看出产生H2应为3×0.9n mol=2.7n mol。
(3)CO2为气体,加压有利于平衡右移,利用的是勒夏特列原理。
(4)此题考查了考生对CO2用途的记忆,写任一种用途即可。
(5)合成氨反应是一可逆反应,H2和N2的转化率低,必须循环利用。