(一)煤的干馏
1、组成成分
煤是由多种有机物和无机矿物质组成的复杂混合物。主要含有 C、H元素外,还含有少量的N、S、O等元素;混合物中的无机化合物里含有Si、Al、Ca、Fe等元素。
2、分类
无烟煤、烟煤、褐煤、泥煤等。
3、干馏
把煤隔绝空气加强热使其分解的过程叫做煤的干馏。
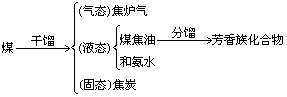
4、气化、液化
煤的气化是把煤中的有机物转化为可燃性气体的过程。

煤的液化是把煤转化成液体燃料的过程。
通过煤的气化和液化可以使煤变成清洁能源,并且提高煤的燃烧率。
5、比较干馏、蒸馏、分馏的差别
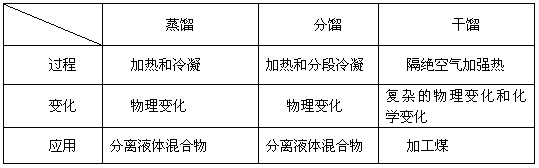
6、煤的综合利用
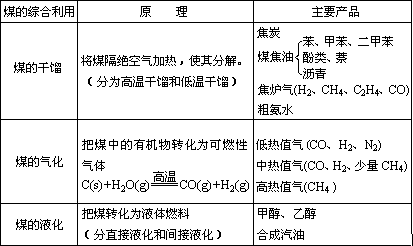
(二)乙炔的结构和组成
分子式: C2H2
电子式: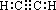
结构式: H―C≡C―H
结构简式: CH≡CH
分子模型: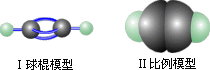
键角 180°,空间上四个原子在同一直线上。
(三)乙炔的实验室制法
1、反应原理:CaC2+2H2O→CH≡CH↑+Ca(OH)2
2、可用排水法收集乙炔气体,一般不用排空气法收集,因为C2H2的密度略小于空气。
3、注意事项:
(1)电石和水反应很剧烈,为得到平稳的乙炔气流,可用饱和食盐水代替水,并选用分液漏斗控制水流的速度。
(2)制取乙炔气体不能用启普发生器,因为:a.电石跟水反应生成Ca(OH)2溶解度较小,容易沉积在容器底部而堵塞球形漏斗下端管口。b.碳化钙与水反应很剧烈,不易控制。c.反应过程中放出大量的热,易使启普发生器炸烈。
(3)工业上生产电石用下面的反应:
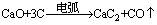
这样制得的 CaC2往往含有CaS、Ca3P2,因此制得的乙炔气体往往含有H2S、PH3等而有臭味。
(四)乙炔的化学性质
1、氧化反应
(1)可燃性:
(2)与酸性KMnO4反应,使酸性KMnO4褪色。
2、加成反应
(1)与Br2的CCl4溶液反应
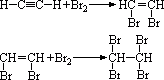
还可以与溴水反应发生加成反应。
(2)与其它物质反应:
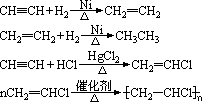
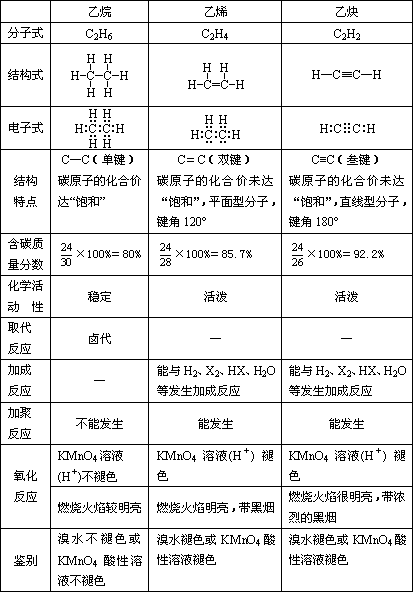
(五)乙烷、乙烯、乙炔分子结构和化学性质的比较
(六)炔烃
1、炔烃的通式为CnH2n-2,这与二烯烃的通式相同
2、炔烃的命名步骤:
(1)选主链:选含有C≡C的最长碳链作为主链,命名为某炔;
(2)编号:从离C≡C最近的一端开始编号;
(3)最后写上取代基的位置、数目和名称,以及C≡C的位置和数目。
3、炔烃的性质
四个碳以下的炔烃为气态烃,炔烃的熔沸点、密度随着碳原子数的增加而升高,炔烃分子中含有叁键,与乙炔的性质相似,可以发生氧化反应和加成反应。