A 卷
开始测试
B 卷
二、综合题
11、A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3中的一种。
① A与B反应有气体生成 ② B与C反应有沉淀生成
③ C与D反应有沉淀生成 ④ D与E反应有沉淀生成
⑤ A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是____________________。
(2)A是_________,B是_________,C是_________,D是_________,E是_________。
(3)A与E反应的离子方程式是_______________________________________。
[答案]
12、有6种白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、碳酸铵、无水硫酸铜、碳酸钠。现只提供蒸馏水,通过下面的实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察的现象是_______________________
检验出的物质的化学式(分子式)是_________________________________
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是
1支试管中有白色沉淀生成___________________________________________;
2支试管中有蓝色沉淀生成___________________________________________。
被检出的物质的化学式(分子式)是________________________________
(3)鉴别余下未检出物质的方法和观察到的现象是_________________________________________________
[答案]
13、某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器有______________(填代号、限填3项)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三角架
E.泥三角 F.酒精灯 D.烧杯 H.量筒
(2)第2步:I-溶液的获取。操作是_____________________________。
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用___________(填代号)。
A.浓硫酸 B.新制氯水 C.KMnO4溶液 D.H2O2
理由是________________________________________。
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
[答案]
14、化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3,和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)。
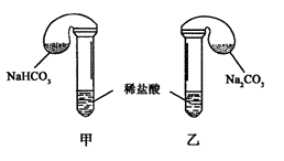
请回答:
(1)各组反应开始时,_____________装置中的气球体积先变大,该装置中反应的离子方程式是_________________________。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
|
试剂用量 |
实验现象 |
分析原因 |
第①组 |
0.42 g NaHCO3
0.53 g Na2CO3
3 mL 4 mol / L盐酸 |
甲中气球与乙中气球的体积相等 |
甲、乙盐酸均过量
n(NaHCO3)=n(Na2CO3)
V甲(CO2)= V乙(CO2) |
第②组 |
0.3 g NaHCO3
0.3 g Na2CO3
3 mL 4 mol / L盐酸 |
甲中气球比乙中气球的体积大 |
|
第③组 |
0.6 g NaHCO3
0.6 g Na2CO3
3 mL 2 mol / L盐酸 |
甲中气球比乙中气球的体积大 |
|
片刻后,乙中气球又缩小,甲中气球的体积基本不变 |
(用离子方程式表示) |
[答案]
15、研究性学习小组进行SO2的制备及性质探究实验。
(1)根据反应Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O,制备SO2气体。
①用下列简图,在答题卡的方框中画出制备并收集SO2的实验装置(含试剂)示意图。
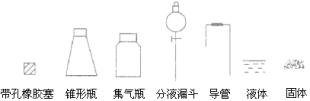
②实验过程中,使用分液漏斗滴加浓硫酸的操作是_____________________________。
(2)将SO2气体分别通入下列溶液中:
①品红溶液,现象是___________________________________________;
②溴水溶液,现象是___________________________________________;
③硫化钠溶液,现象是_________________________________________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)。
①原因__________________,验证方法____________________________________。
②原因__________________,验证方法____________________________________。
③原因__________________,验证方法____________________________________。
[答案]
|