| 高考第一轮化学
单元训练题八 碳族元素 无机非金属材料
|
|
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共108分,考试时间100分钟。
可能用到的相对原子质量:H:1 O:16 C:12 N:14 Si:28 Na:23 K:39
Ca:40 Al:27 Mg:24
第Ⅰ卷(选择题,共46分)
一、选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
1、下列物质中,不含有硅酸盐的是( )
A.水玻璃 B.硅芯片
C.黏土 D.普通水泥
2、下列表述正确的是( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④
C.③④⑤ D.③⑤
3、下列说法中不正确的是( )
A.SiO2是酸性氧化物,它不与任何酸反应
B.锗是两性元素,但其金属性比非金属性强
C.硅的化学性质不活泼,常温下与氧气、氯气、浓硫酸、硝酸等强氧化剂均不反应
D.SiO2和CO2在物理性质上有很大差别
4、Na2SiO3与Na2CO3的共同性质是( )
①易溶于水 ②水溶液能与CO2作用
③与稀硫酸发生复分解反应 ④水溶液有粘接性能
A.④ B.①②③
C.除②外 D.①②③④
5、金属陶瓷是一种应用于高科技的复合材料,合成方法是将陶瓷(主要成分为Al2O3、ZrO2等耐高温材料)和粘结金属(主要是Cr、Mo、W、Ti等高熔点金属)研磨混匀成型后,高温烧结使金属仍然以单质的形式存在于金属陶瓷之中,据此判断合成工艺必须( )
A.在氧气中合成 B.在HCl气氛中合成
C.在氮气气氛中合成 D.在空气中合成
6、汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确是( )
A.用盐的形式表示:BaSiO3·CuSiO3
B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
7、某无色混合气体可能含有CO2、CO、H2O(水蒸气)、H2中的一种或几种,依次进行如下处理(假定每次处理均反应完全):①通过碱石灰时,气体体积变小;②通过赤热的氧化铜时,固体变为红色;③通过白色硫酸铜粉末时,粉末变为蓝色;④通过澄清石灰水时,溶液变浑浊。由此可以确定原混合气体中( )
A.一定含有CO2、H2O,可能含有H2、CO中的一种
B.一定含有H2O、CO,可能含有CO2、H2O中的一种
C.一定含有CO、CO2,可能含有H2O、H2中的一种
D.一定含有CO、H2,可能含有H2O、CO2中的一种
8、某玻璃中含Na2O、CaO、SiO2的质量比约为10︰9︰58,则玻璃的组成为( )
A.Na2O·CaO·6H2SiO3
B.Na2O·CaO·6SiO2
C.2Na2O·2CaO·9SiO2
D.5Na2O·6CaO·SiO2
二、(本题包括10小题,每小题3分,共30分。每小题有一个或两个选项符合题意,若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的得1分,选两个且都正确的得3分,但只要选错一个,该小题就为0分)
9、下列说法正确的是( )
A.硅材料广泛用于光纤通讯
B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.粗硅制备单晶硅不涉及氧化还原反应
10、门捷列夫在19世纪中叶,曾根据他所发现的规律,预言过第四周期ⅣA族元素X(当时他称为类硅),下列有关该元素的性质不正确的是( )
A.XH4不稳定,但有强还原性
B.可用焦炭在高温下从XO2中冶炼X
C.X单质的熔点比硅高
D.最高价氧化物对应水化物化学式为X(OH)4,其酸性较H2SiO3强
11、在雷达的微波过滤器里使用的铁氧磁性体,如钇铁石榴石Y3Fe5O12,其中钇(Y)是ⅢB族稀土元素。下面有关叙述中正确的是( )
A.可表示为3YO3·3FeO·Fe2O3
B.可表示为Y3O5·Fe3O4·Fe2O3
C.其中钇、铁的化合价均为+3价
D.其中钇、铁的化合价均有+2、+3价
12、下列反应中,能说明碳元素的非金属性比硅元素强的是( )
A.SiO2+2C Si+2CO↑ Si+2CO↑
B.CaCO3+SiO2 CaSiO3+CO2↑ CaSiO3+CO2↑
C.Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓
D.Si+4HF=SiF4+2H2
13、工业上由粗硅制纯硅有以下反应
①Si(s)+3HCl(g) 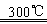 SiHCl3(g)+H2(g);△H<0 SiHCl3(g)+H2(g);△H<0
②SiHCl3(g)+H2(g)  Si(s)+3HCl(g) Si(s)+3HCl(g)
对上述反应的说法中正确的是( )
A.均为置换反应和氧化一还原反应
B.反应①②实际上互为可逆反应
C.由于反应①放热,则反应②一定吸热
D.提高SiHCl3产率,应采用加压和升温的方法
14、下列各组离子能大量共存的是( )
A.HCO3-、NH4+、H+、Ca2+
B.SiO32-、H+、Cl-、NO3-
C.K+、SiO32-、Na+、CO32-
D.Mg2+、OH-、SiO32-、H+
15、人们研究金星大气成分,发现金星大气中有一种称之为硫化羰(化学式为COS)的分子,已知硫化羰与二氧化碳的结构相似,硫化羰是一种与生命密切相关的物质,下列说法中错误的是( )
A.COS分子是含有极性键的极性分子
B.COS分子所有原子都满足8电子稳定结构
C.COS分子不能发生加成反应
D.COS分子中3个原子处于同一直线上
16、氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是( ) 2AlN+3CO合成。下列叙述正确的是( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1molAlN需转移3mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
17、根据碳族元素的相似性与递变性、一般性与特殊性的知识,判断下列说法正确的是( )
A.CO2、PbO2都是强氧化剂
B.CO2和PbO2都是弱氧化剂,CO和PbO都是还原剂
C.Sn(OH)4可与NaOH反应,但不与盐酸反应
D.Ge单质的熔点介于Si、Pb之间,是半导体材料
18、二氧化硅晶体具有立体网状结构,其晶体模型如图8-1所示。对于二氧化硅晶体的说法正确的是( )
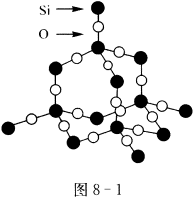
A.二氧化硅晶体最小环为12元环
B.每个硅原子为4个最小环所共有
C.从晶体结构可知,1mol SiO2拥有2mol Si—O键
D.每个最小环平均拥有6个氧原子
[提示]
第Ⅱ卷 (共62分)
三、(本题包括2小题,共16分)
19、(7分)碱式碳酸镁有多种不同的组成,如:Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等。某研究性学习小组的同学们为了确定某碱式碳酸镁的组成,设计了如图8-2所示的实验装置。
(1)实验步骤:
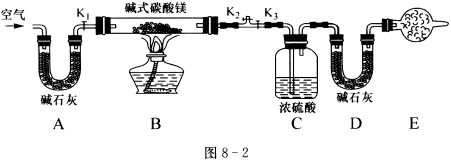
①按图8-2(夹持仪器未画出)组装好装置后,首先进行的操作是__________,E处干燥管盛放的药品是__________。
②称取碱式碳酸镁样品m1 g,并将其放入硬质玻璃管中,称量:装浓硫酸的洗气瓶C的质量为m2 g,装碱石灰的U形管D的质量为m3 g。
③打开活塞__________,关闭__________,缓缓鼓入空气数分钟。
④关闭活塞__________,打开__________,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称量得洗气瓶C的质量为m4g;U形管D的质量为m5 g。实验测得数据如下:m1=31,m2=87.7,m3=74.7,m4=89.4,m5=87.9,计算推导:该碱式碳酸镁的化学式为__________。
(2)关于该实验方案。以下说法你认为正确的是__________ (填字母)。
A.硬质玻璃管中有水凝结对测定结果会产生较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O)(a、b、c为正整数)]的化学组成
20、(9分)晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl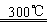 SiHCl3+H2; SiHCl3+H2;
③SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为______________________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为__________。
(3)用SiHCl3与过量H2反应制备纯硅的装置如图8-3所示(热源及夹持装置略去):
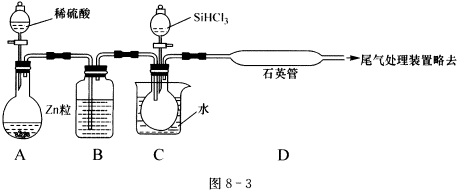
①装置B中的试剂是__________,装置C中的烧瓶需要加热,其目的是____________________。
②反应一段时间后,装置D中观察到的现象是__________,装置D不能采用普通玻璃管的原因是__________,装置D中发生反应的化学方程式为__________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及______________________________。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是__________。
a.碘水 b.氯水 c.NaOH溶液
d.KSCN溶液 e.Na2SO3溶液
[答案]
四、(本题包括2小题,共17分)
21、(11分)阅读材料,回答有关问题。
(1)铅的主要化合价是+2价和+4价,+4价铅元素的化合物是不稳定的,+4价铅元素的化合物有强氧化性。例如PbO2的氧化性比Cl2的强。Pb3O4中铅表现为+2价和+4价。写出Pb3O4与浓盐酸反应的化学方程式______________________________。
(2)锡为ⅣA族元素,锡的单质和化合物与某些物质在化学性质上有许多相似之处。
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应的变化,试写出有关反应的化学方程式____________________。
②将①中溶液蒸干后继续加热所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是(写化学式) ____________________。
③若向①中所得溶液中加入适量的NaOH溶液,产生白色沉淀(该沉淀物的分子中含2个氢原子),再加过量的NaOH溶液,白色沉淀溶解。上述反应类似于AlCl3溶液的相应反应,试写出有关反应的离子方程式____________________。
(3)把河沙(主要成分是SiO2)跟镁粉按一定质量比(质量比大于15︰24)混合均匀,加热后发生剧烈反应,生成一种白色固体化合物和一种硅化物。待生成的混合物冷却后加入稀硫酸,立即产生气泡并伴有爆炸声,产生的气体是一种能在空气中自燃的气态氢化物。
①写出河沙与镁粉在加热条件下的化学方程式____________________。
②写出产生“爆炸声”的化学方程式____________________。
(4)在氮化硅中添加氧化铝,用氧原子替代一部分氮,用铝原子替代一部分硅,通过常压烧结即成新一代无机非金属材料,叫氧氮化硅铝,即赛伦(Sialon),化学通式为:Si6-xAlxOxNy(x:2~4)。则
①判断赛伦属__________晶体类型,并且有____________________等特性(至少写三种)。
②化学通式里的y值为__________ (用含x的表达式或某一具体数值表示)。
22、(6分)(1)在石油化工的加氢操作中,如果氢气中混有CO和CO2等杂质,会引起催化剂中毒,因此必须除去。
①在常温下,可以用银氨溶液来检测微量的CO,其原理与银镜反应相似,有银析出。写出银氨溶液与CO反应的化学方程式____________________。
②工业上常用甲烷化法除去少量碳的氧化物(CO、CO2)。其方法是:一定温度时,在催化剂的作用下,向碳的氧化物中通入氢气,使之转化为甲烷和易于除去的水。写出CO发生甲烷化反应的化学方程式____________________。
③在上述两个反应中,CO依次作__________、__________。
A.氧化剂
B.既是氧化剂,又是还原剂
C.还原剂
D.既不是氧化剂,又不是还原剂
(2)航天飞行器座舱内空气更新过程如图8-4所示:
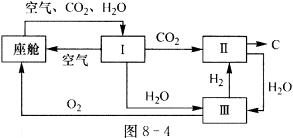
①Ⅱ是CO2和H2的反应装置,该反应的化学方程式是____________________。
②从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,宇航员每天消耗28mol O2,呼出23mol CO2,则宇航员每天呼出的气体中含H2O__________mol。
[答案]
五、(本题包括2小题,共16分)
23、(7分)图8-5所示为各单质和化合物之间的转化关系,而且各单质和化合物的组成元素皆为短周期元素。
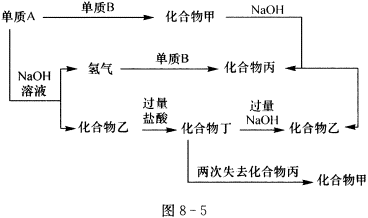
根据上述关系判断:
(1)单质A只可能是__________,这是因为____________________。
(2)各化合物的化学式:甲__________,乙__________,丙__________,丁__________。
(3)写出单质A与NaOH溶液反应的化学方程式并标出电子转移的方向和数目:____________________。
24、(9分)材料科学是近年来与化学有关的科学研究的热点。某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性。它是以中学化学中的常见物质为原料来生产的,图8-6中虚线框外为其生产过程;虚线框内的其他转化是为探究C的组成而设,F、H均为难溶于水的白色固体;图8-6中C、M、K均含A元素,其余物质均为中学化学中常见的物质。
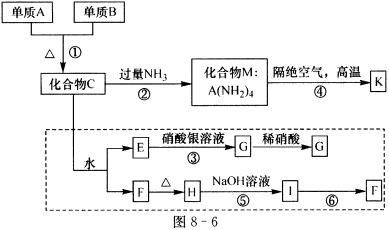
请回答下列问题:
(1)指出K可能所属的晶体类型__________,K中A原子周围化学键之间的夹角均相等,化学键之间的夹角为__________。
(2)写出化学式:化合物C__________,化合物F__________。
(3)写出反应的离子反应方程式:
③________________________________________;
⑤________________________________________。
(4)写出反应④的化学反应方程式______________________________。
(5)K抗腐蚀能力强,除氢氟酸外,它不跟其他无机酸反应,试推测K被氢氟酸腐蚀的化学方程式____________________。
(6)现用C和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的K,反应的化学方程式为______________________________。
[答案]
六、(本题包括2小题,共13分)
25、(6分)地球化学中,通常用热重分析研究矿物在受热时的质量变化以确定其组成。取66.6mg由高岭石[Al4Si4O10(OH)8]和方解石(CaCO3)组成的矿物,加热,在673~1123K区间内分解为氧化物,样品总失重13.8mg。
(1)方解石的失重百分比为多少。
(2)计算矿物中高岭石的质量分数。
[答案]
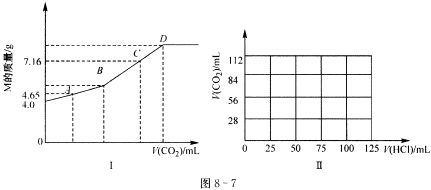
26、(7分)往200mL NaOH溶液中通入CO2,充分反应后,在减压和低温下,小心将溶液蒸干,得白色固体M。通入CO2的体积V(CO2)(mL)(标准状况下)与M的质量(g)的关系如图8-7Ⅰ所示。试通过分析和计算回答下列问题(要求写出简要计算过程):
(1)B点时,白色固体M的化学式为__________,通入CO2的体积为__________mL。
(2)D点时,通入CO2的体积为__________mL。
(3)C点时,通入CO2的体积为__________mL。
(4)取组成为A点的白色固体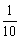 ,向其中逐滴加入0.1mol·L-1 HCl溶液,请在图8-7Ⅱ中画出产生CO2气体体积(标准状况下)与所加入的盐酸的体积关系。 ,向其中逐滴加入0.1mol·L-1 HCl溶液,请在图8-7Ⅱ中画出产生CO2气体体积(标准状况下)与所加入的盐酸的体积关系。
[答案]
- 返回 -
|







