|
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共108分,考试时间100分钟。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Cu:64 S:32 P:31
Ca:40 Fe:56 Cu:64 Ba:137
第Ⅰ卷(选择题,共46分)
一、选择题(本题包括8小题,每小题2分,共16分。每小题只有一个选项符合题意)
1、关于氮气性质的说法中,错误的是( )
A.通常情况下,氮气的性质很不活泼
B.可在氧气中燃烧,生成一氧化氮
C.在水中溶解度小(通常状况下)
D.跟氢气在一定条件下发生反应,氮气是氧化剂
2、关于氮族元素的叙述正确的是( )
A.它们的单质在常温下都难以与H2化合
B.它们单质的熔沸点从氮到铋依次升高
C.它们最高价含氧酸的化学式都可用H3RO4表示
D.它们最高价氧化物对应的水化物都是强酸
3、下列气体不会造成大气污染的是( )
A.二氧化硫 B.一氧化氮
C.一氧化碳 D.氮气
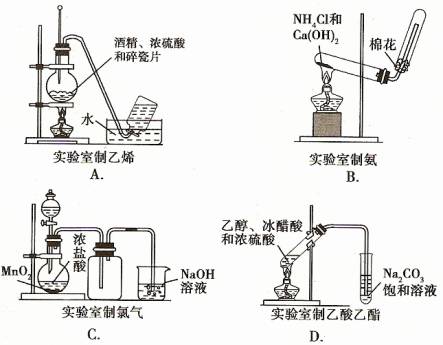
4、下列实验装置图正确的是( )
5、已知气体的摩尔质量越小,扩散速度越快。如图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是( )

A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸
D.甲是浓硝酸,乙是浓氨水
6、下列氧化物中,不是酸酐的是( )
A.N2O5 B.NO
C.N2O3 D.P2O5
7、某集气瓶内气体呈红棕色,加入足量水,盖上玻璃片振荡,得棕色溶液,气体颜色消失;打开玻璃片后,瓶中气体又变为红棕色,则该气体可能是下列混合气体中的( )
A.N2、NO2、Br2(g) B.NO2、NO、N2
C.NO2、NO、O2 D.N2、O2、Br2
8、在一定温度下,将盛满N2和NO2混合气体的试管如图9-1所示倒立在水槽中,经足够长时间后,试管内的气体的体积缩小为原体积的3/5,则原混合气体中N2和NO2的体积比为( )
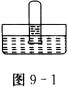
A.3︰2 B.2︰3
C.5︰3 D.3︰5
二、(本题包括10小题,每小题3分,共30分。每小题有一个或两个选项符合题意,若正确答案只包括一个选项,多选时该小题为0分;若正确选项包括两个选项,只选一个且正确的得1分,选两个且正确的得3分,但只要选错一个,该小题就为0分)
9、下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
A.漂白粉的成分为次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH溶液处理NO2和HCl废气
D.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒
10、Cu2S与一定浓度的HNO3反应生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2与NO的物质的量之比为1︰1时,实际参加反应的Cu2S与HNO3的物质的量之比为( )
A.1︰7 B.1︰9
C.1︰5 D.2︰9
11、下图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶管的胶头,下列与试验事实不相符的是( )
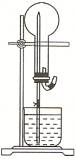
A.CO2(NaHCO3溶液); 无色喷泉
B.NH3(H2O含酚酞); 红色喷泉
C.H2S(CuSO4溶液); 黑色喷泉
D.HCl(AgNO3溶液); 白色喷泉
12、将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),则所消耗硝酸的物质的量是( )
A.0.12mol B.0.11mol
C.0.09mol D.0.08mol
13、检验某盐溶液中是否含有NH4+的方法是:将待测溶液取出少许,放在试管中,然后( )
A.加热,用湿润的红色石蕊试纸置于试管口检验
B.加烧碱溶液后加热,再滴入无色酚酞试液
C.加热,用蘸有浓硫酸的玻璃棒置于试管口检验
D.加烧碱溶液后加热,再用湿润的红色石蕊试纸置于试管口检验
14、相同状况下,在容积相同的三个烧瓶内分别充满干燥的NH3、HCl、NO2气体,然后按上述顺序分别用水做喷泉实验。实验结束后,烧瓶内三种溶液的物质的量浓度之比为( )
A.3︰3︰2 B.2︰2︰3
C.1︰1︰1 D.无法比较
15、研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2 SO3+NO , ②SO3+H2O SO3+NO , ②SO3+H2O H2SO4, ③2NO+O2 H2SO4, ③2NO+O2 2NO2 2NO2
NO2在上述过程中的作用,与H2SO4在下述变化中的作用相似的是( )
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.硫化氢通入浓H2SO4
C.浓H2SO4滴入萤石中,加热
D.加入少量的H2SO4使乙酸乙酯水解
16、在某100mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4mol·L-1和
0.1mol·L-1。向该混合液中加入1.92g铜粉,加热,待充分反应后。所得溶液中的Cu2+的物质的量浓度(mol·L-1)是( )
A.0.15 B.0.225
C.0.35 D.0.45
17、下列物质间发生的化学反应在不同条件下生成物亦不同的是( )
①NaCl(s)和浓H2SO4 ②H2S和O2 ③Na和O2 ④Fe和稀盐酸 ⑤Cu和硝酸 ⑥P2O5和水
A.①②③⑤⑥ B.①②③④⑤
C.①③⑤⑥ D.①②⑤⑥
18、将磷酸溶液逐滴加到60mL的氢氧化钡溶液中,其溶液的pH与所加磷酸溶液的体积之间的关系如图9-2所示(溶液的总体积看作原溶液体积与加入的溶液体积之和)。则下列说法正确的是( )
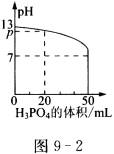
A.磷酸的物质的量浓度是0.05mol·L-1
B.pH为7时,生成1.2g沉淀
C.pH为p时,生成0.24g沉淀
D.pH为p时,溶液中的c(OH-)为0.045mol·L-1
[提示]
第Ⅱ卷 (共62分)
三、(本题包括2小题,共18分)
19、(8分)A~D是中学化学实验常见的制备气体的实验装置示意图(图9-3)。回答下列问题:
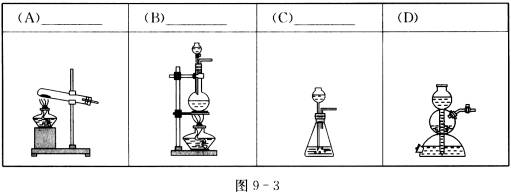
(1)实验室制备下列气体,把编号填入最适宜的图(A)~(C)旁的横线上。
①H2S ②O2 ③H2 ④CO2 ⑤NH3 ⑥HCl ⑦Cl2
(2)选用装置D制备气体之前应怎样检查其气密性?________________________
20、(10分)为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图9-4所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
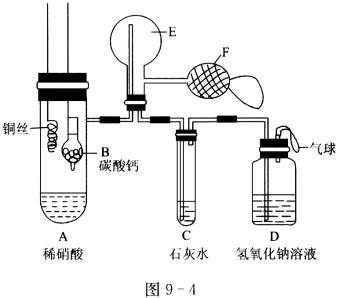
(1)实验时,先将B装置下移,使碳酸钙和稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的是________________________________________________________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为________________。
装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是________________________;
一段时间后,C中白色沉淀溶解,其原因是________________________。
(3)装置D的作用是________________________________。
[答案]
四、(本题包括2小题,共17分)
21、(8分)图9-5表示A、B、C、D、E五种含氮物质相互转化的关系图。其中A、B、C、D常温下都是气体,D为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式。
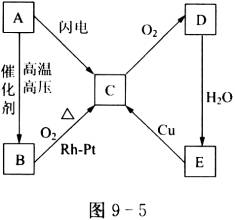
(1)各物质的化学式为:A.__________,B.__________,C.__________,D.__________,E.__________。
(2)各步反应的化学方程式为:
A→C:__________________________________________________;
B→C:__________________________________________________;
D→E:__________________________________________________;
E→C:__________________________________________________。
22、(9分)A、B、C、D均为短周期元素,A和B是同周期相邻的两种元素,A和C是同主族相邻的两种元素;A、B、C三种元素的原子序数之和为31;D元素与A、B、C三种元素均不同周期,也不同主族。请回答:
(1)C元素的名称是____________________。
(2)A、B、D可组成化学式为D4B2A3的离子化合物,其水溶液呈酸性,原因是(用离子方程式表示) ________________________________________。
(3)B、D形成的化合物液态时可发生微弱电离(电离过程与D2A的电离相似),电离产生的阴离子的电子式为____________________。
(4)已知:BA2+A2+D2A→DBA3。如图9-6所示,若将一充满m mL BA2和A2混合气体的大试管倒立于D2A中,充分反应后,在相同条件下测得试管中余下n mL气体,则:
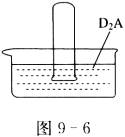
①若余下n mL气体为__________,原混合气体中BA2的体积为__________mL,A2的体积为__________mL。
②若余下n mL气体为__________,原混合气体中BA2的体积为__________mL,A2的体积为__________mL。
[答案]
五、(本题包括2小题。共12分)
23、(8分)亚磷酸H3PO3是一种无色晶体,有大蒜气味、强吸湿性。
(1)在亚磷酸溶液中加入过量的氢氧化钠溶液,生成的主要产物是Na2HPO3,这一实验事实可证明亚磷酸是几元酸? ________,试写出亚磷酸的电离方程式__________________。
(2)亚磷酸具有还原性,当它与碘水混合后,可以看到碘水的棕黄色褪去,并有H3PO4生成,写出有关化学方程式____________________。
(3)在亚磷酸溶液中加入AgNO3后,有黑色沉淀生成并且生成无色气体,该无色气体在试管口变成红棕色。写出有关化学方程式____________________。
24、(4分)多硫化物Sx2-(x=2~6)在碱性溶液中被BrO3-氧化为SO42-,而BrO3-被还原成Br-。在反应中,消耗BrO3-和OH-的物质的量之比为2︰3,则x值为__________,其反应的离子方程式为____________________。
[答案]
六、(本题包括2小题,共15分)
25、(9分)将10g铁置于40mL某浓度的硝酸中。微热使其充分反应,随着反应的进行,硝酸的浓度降低,生成气体的颜色由红棕色变为无色,反应至最后共收集到1792mL NO2和NO的混合气体(均为标准状况,不考虑N2O4存在),最后溶液中尚余4.4g固体。求:
(1)该反应中被还原的HNO3与未被还原的HNO3的质量之比。
(2)原硝酸的物质的量浓度。
(3)生成的混合气体中NO与NO2的体积比。
[答案]
26、(6分)有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀;滤液与4.0mol·L-1的NaOH溶液反应,用去35mL碱液时恰好完全中和。试求:
(1)原混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液,加入3.2g铜粉共热时,在标准状况下收集到气体的体积为多少毫升?
[答案]
- 返回 -
|









