(1)自身氧化还原反应方程式,一般先从生成物开始配平(即逆向配平)较为方便。
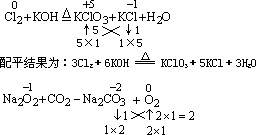
配平结果为:2Na2O2+2CO2=2Na2CO3+O2
(2)反应物中某一物质部分被氧化(或被还原)的氧化还原反应,一般从生成物开始配平(即逆向
配平)较为方便。
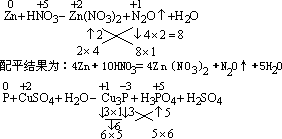
配平结果为:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4
(3)一般的物质间的氧化还原反应,由反应物或生成物开始配平都行。
(1)化学方程式所表示的是纯净物之间的量的关系,因此不纯物质或溶液应先换算成纯物质的量,才可进行计算。
(2)在所列比例中,同一物质上下单位一致,不同物质左右单位要相当。
(3)有关反应物过量的相关计算,应先判断哪种反应物过量,再用不过量的那种反应物的量来计算。
有关多步反应的相关计算,建立量的关系时,可用关系式法、元素守恒法,并注意,物质的物质的量之比不一定等于1:1。
有一种反应物过量的计算
过量计算的方法:设一反应物的量为未知量x,由另一种反应物的已知量求出x,再将x值与题中已知量进行比较,若计算出的x值比题中给出的量小,表明此反应物过量,应以另一种反应完全的物质为标准进行计算;若计算出来的x值比题给出的量大,表明此反应物少量,应以该反应物的量进行计算。
多步反应的计算
(1)多步反应的解题步骤
①写出各步反应的化学方程式;
②根据化学方程式找出可以作为中介的物质,并确定最初反应物、中介物质、最终生成物之间的
量的关系;
③确定最终反应物和最终生成物之间的量的关系;
④根据所确定的最初反应物和最终生成物之间的量的关系和已知条件进行计算。
(2)物质的纯度、原料的利用率(或转化率)、产物的产率的计算方法。

①利用率是相对反应物而言,产率是对生成物而言。
②在解题时,往往遇到原料或中间物质不能全部转化的情况,常进行如下处理。
某一种化合物中元素的损失率=该化合物的损失率
中间产物的损失率=原料的损失率
中间产物的转化率=原料的转化率
(3)建立最初反应物和最终生成物之间的量的关系的方法
关系式法:先写出多步反应的化学方程式(要配平),然后找出反应物和生成物之间物质的量之比,列出关系式。
元素守恒法:原料中某一关键元素理论上若全部转入产物中,则该元素的原子个数在两种物质中应相等,据此列出关系式。
如:工业制HNO3
4NH3+5O2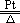 4NO+6H2O
4NO+6H2O
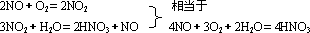
①由关系式可得NH3~NO~HNO3
②由氮元素守恒得NH3~HNO3
工业制H2SO4:
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
2SO2+O2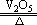 2SO3
2SO3
SO3+H2O=H2SO4
①由关系式法可得:FeS2~2SO2~2SO3~2H2SO4
②由硫元素守恒得FeS2~2H2SO4
课本上例题4的另一种解法为:
解:设可制得98%硫酸的质量为x
由4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
2SO2+O2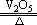 2SO3
2SO3
SO3+H2O=H2SO4
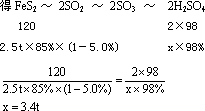
答:可制得98%硫酸3.4t。