1、下列离子方程式书写正确的是( )
A.向明矾溶液中滴加Ba(OH)2溶液至Al3+恰好完全沉淀:
Al3++2SO42-+3OH-+2Ba2+=2BaSO4↓+Al(OH)3↓
B.向明矾溶液中滴加Ba(OH)2溶液至SO42-恰好完全沉淀:
2Al3++SO42-+Ba2++4OH-= BaSO4↓+AlO2-+2H2O
C.向FeI2溶液中通入Cl2至I-恰好完全被氧化:
2I-+Cl2= I2+2Cl-
D.向FeI2溶液中通入Cl2至恰好完全被氧化:
2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-。
2、下列离子方程书写正确的是( )
A.Fe3+的检验Fe3++3SCN-=Fe(SCN)3↓
B.Na2S溶液呈碱性S2-+2H2O= H2S+2OH-
C.金属钠与水反应2Na+2H2O=2Na++2OH-+H2↑
D.FeS固体放入稀硝酸溶液中FeS+2H+=Fe2++H2S↑
3、向含有NH4+、Mg2+、Fe2+和Al3+的溶液中加入足量Na2O2微热并搅拌后,再加入过量稀盐酸,溶液中大量减少的离子是( )
A.NH4+
B.NH4+、Fe2+
C.Al3+、Mg2+
D.Al3+
4、某溶液中可能会有I-、NH3+、Na+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于该溶液组成的判断正确的是( )
①肯定有I- ②肯定不含Na+
③肯定含SO32- ④可能含I-
A.①③
B.①②③
C.③④
D.②③④
5、下列反应的离子方程式书写正确的是( )
A.向氢氧化钡溶液中逐滴加入少量碳酸氢镁溶液 Ba2++2OH-+2HCO3- BaCO3↓+2H2O
BaCO3↓+2H2O
B.向亚硫酸钠溶液中逐滴加入少量氯水 SO32-+Cl2+ H2O SO42-+2H++2Cl-
SO42-+2H++2Cl-
C.用醋酸溶液吸收氨气 H++NH3 NH4+
NH4+
D.镁粉溶于氯化铵溶液 Mg+2NH4++2H2O Mg2++2NH3・H2O
Mg2++2NH3・H2O
6、(2004,年江苏)下列反应的离子方程式书写正确的是()
A.硫酸铝溶液中加入过量氨水
Al3++3OH-=Al(OH)3↓
B.电解饱和食盐水
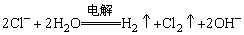
C.碳酸钙与盐酸反应
CaCO3+2H+=Ca2++ CO2↑+2H2O
D.硫酸亚铁的溶液中加入用硫酸酸化的过氧化氢溶液
Fe2++2H++H2O2=Fe3++2H2O
7、(2004年,广东)下列离子方程式中,正确的是()
A.向氯化亚铁溶液中通入氯气,Fe2++Cl2=Fe3++2Cl-
B.三氯化铁溶液跟过量氨水反应,Fe3++3NH3・H2O=Fe(OH)3↓+3NH4+
C.碳酸氢钙溶液跟稀硝酸反应,Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑
D.氯气通入冷的氢氧化钠溶液中,2Cl2+2OH-=3Cl-+ClO-+H2O
8、下列物质加入水中显著地放热的是( )
A.固体氢氧化钠
B.生石灰
C.无水乙醇
D.固体硝酸铵
9、下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应放热还是吸热
D.吸热反应在一定条件下(如常温、加热等)也能发生反应
10、(2004年,浙、赣、闽等8省理综)下列离子方程式正确的是()
A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O
B.钠与水的反应Na+2H2O=Na++2OH-+H2↑
C.铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag
D.大理石溶于醋酸的反应CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O