(一)原子结构
构成原子的粒子 |
电子 |
原子核 |
质子 |
中子 |
电性和电量 |
1个电子带1个单位负电荷 |
1个质子带1个单位正电荷 |
不显电性 |
质量/kg |
9.109×10-31 |
1.673×10-27 |
1.675×10-27 |
相对质量 |
质子质量的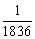 |
1.007 |
1.008 |
构成原子的粒子及其性质
原子是由居于原子中心的带正电的原子核和核外带负电的电子构成的,而原子核是由带正电的质子和不显电性的中子构成的。
原子核所带电量跟核外电子带的电量相等而电性相反,因此原子作为一个整体不显电性。
原子很小,原子核更小,它的半径约为原子半径的几万分之一,体积是整个原子的几千亿分之一,原子核虽小,但它聚集了几乎整个原子的所有质量。
说明:
(1)中子比质子略重;电子的质量很小,可忽略。
(2)中子数、质子数约等于中子、质子的相对质量。
以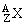 代表一个质量数为A、质子数为Z的原子:
代表一个质量数为A、质子数为Z的原子:

(二)构成原子或离子的粒子间的关系
1、对于原子
质量关系:质量数(A)=质子数(Z)+中子数(N)
电性关系:核电荷数(Z)=质子数(Z)=核外电子数=原子序数
2、对于离子
阳离子:质子数>核外电子数;电荷数=质子数-阳离子核外电子数
阴离子:质子数<核外电子数;电荷数=阴离子核外电子数-质子数
3、对于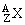 ,X原子的相对原子质量近似等于质量数。
,X原子的相对原子质量近似等于质量数。
4、并不是任何原子核都是由质子和中子构成,如: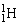 。
。
(三)构成原子的基本微粒特点
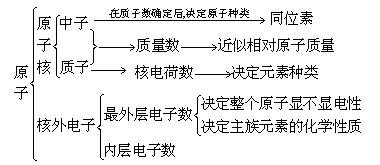
(四) 核素和同位素
1、元素:具有相同核电荷数(即质子数)的一类原子的总称。
2、核素:具有一定数目的质子和一定数目的中子的一种原子,叫做核素。如氢元素有三种核素: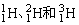 ;如氧元素有三种核素:
;如氧元素有三种核素: 。
。
3、同位素:质子数相同而中子数不同的同一元素的不同核素之间互称同位素,如氢有三种同位素: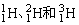 ;氧有三种同位素
;氧有三种同位素 ;碳的同位素有
;碳的同位素有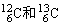 等。
等。
4、同位素的两个重要特征:
(1)同一元素的各种核素虽然质量数不同,但化学性质几乎完全相同;
(2)天然存在的某种元素,不论游离态还是化合态,各种同位素原子的百分含量(同位素在自然界的丰度)一般是不变的。
(五)原子核外电子排布
1、电子层的表示方法
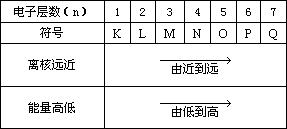
2、原子核外电子分层排布的一般规律
在含有多个电子的原子里,电子依能量的不同分层排布,其规律是:
(1)核外电子总是尽先排布在能量较低的电子层,然后由里到外依次排布在能量逐步升高的电子层能量最低原理)。
(2)原子核外各电子层最多容纳2n2个电子(n为电子层数)。
(3)原子最外层电子数目不能超过8(k为最外层不能超过2个电子)。
(4)次外层电子数目不能超过18个(k层为次外层时不能超过2个),倒数第三层电子数目不能超过32个。
3、结构示意图表示原子、离子结构
(1)原子:核电荷数=核外电子数 例: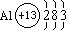
(2)阳离子:核电荷数>核外电子数 例: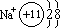
(3)阴离子:核电荷数<核外电子数 例: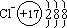
(六)原子的质量、质量数和元素的相对原子质量辨析
1、同位素的相对原子质量
指的是某一种原子的相对原子质量。
例如:已知一个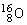 的质量为2.657×10-26kg,一个
的质量为2.657×10-26kg,一个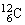 的质量为1.993×10-26kg,
的质量为1.993×10-26kg,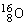 的相对原子质量=
的相对原子质量=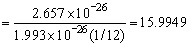
2、原子的质量数
是指某元素的一种同位素原子的核中所含质子数和中子数之和。在数值上可看作原子的近似相对原子质量。
3、元素的相对原子质量
是按各种天然同位素原子的丰度算出来的平均值。
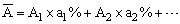
4、元素的近似相对原子质量
上式中的A1、A2、…若用同位素的近似相对原子质量(数值上与质量数相等)代入计算,所得结果即为该元素的近似相对原子质量。
例:已知氯元素有两种天然同位素: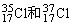 ,并测得以下数值:
,并测得以下数值:
符号同位素的相对原子质量在自然界各同位素的原子百分数
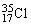 34.969 75.77%
34.969 75.77%
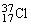 36.966 24.23%
36.966 24.23%
则氯元素的相对原子质量=34.969×75.77%+36.966×24.23%=35.45
氯元素的近似相对原子质量=35×75.77%+37×24.23%=35.48
例1、将有关数字及符号填入下表内:
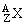
|
核内质子数 |
核外电子数 |
核内中子数 |
质量数 |
| |
20 |
|
|
42 |
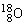
|
|
|
|
|
| |
|
|
14 |
26 |
| |
|
3 |
3 |
|
答案:
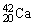 ;20;22;
;20;22;
8;8;10;18;
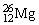 ;12;12;
;12;12;
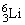 ;3;6
;3;6
解析:
本题考查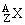 的含义:代表一个质量数为A,质子数为Z的原子,且存在以下关系:质量数(A)=质子数(Z)+中子数(N);核电荷数=质子数=核外电子数。
的含义:代表一个质量数为A,质子数为Z的原子,且存在以下关系:质量数(A)=质子数(Z)+中子数(N);核电荷数=质子数=核外电子数。
例2、在下列原子(或离子)结构简图所表示的微粒中(用元素符号填空)
A.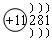 B.
B.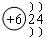
C.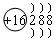 D.
D.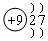
分别写出A、B、C、D所代表的微粒的符号:A_________;B_________;C_________;D_________。
答案:
A:Na; B:C;C:S2-; D:F
解析:
本题主要考查原子结构示意图和离子结构示意图,若核电荷数=核外电子数,即为原子;若核电荷数>核外电子数,即为阳离子;若核电荷数<核外电子数,即为阴离子。
例3、1919年,Langmuir提出的等电子原理:原子数相同,电子总数相同的分子,互称为等电子体,等电子体的结构相似,物理性质相近。
(1)根据上述原理,仅由第二周期元素组成的共价分子中互为等电子体的是:_________和_________;_________和_________。(2)此后,等电子原理又有所发展。例如,由短周期元素组成的粒子,只要其原子数相同,各原子最外层电子数之和相同,也可互称等电子体,它们也具有相似的结构特征,在短周期元素组成的物质中与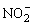 互为等电子体的分子有_________、_________。
互为等电子体的分子有_________、_________。
答案:
(1)N2和CO;N2O和CO2;
(2)O3、SO2
解析:
C、N、O为相邻的连续排列的三个原子,原子序数依次增大1;O、S的最外层均为6个电子。